Tratamiento anaerobio para la remoción de compuestos fenólicos e hidrocarburos saturados
Resumen
Se evaluó la eficiencia de un reactor UASB para la remoción de fenol, 2-clorofenol, 2-nitrofenol, 2,4-dimetilfenol, hexano y heptano de un agua residual preparada en el laboratorio, utilizando glucosa como cosustrato. La carga orgánica volumétrica aplicada varió entre 0,90-5,60 kg DQO/m3 .d, con un TRH de 1 d. Con la aplicación del tratamiento biológico se alcanzaron las siguientes remociones, en los parámetros evaluados: DQO, 81,54%; fenol, 33,65%; 2-clorofenol, 76,60%; 2-nitrofenol, 54,81%; 2,4-dimetilfenol, 77,03%; el hexano y heptano no fueron detectados en el efluente del reactor UASB. La biosorción en lodos y la volatilización de los compuestos orgánicos no fueron evaluadas. La investigación permitió demostrar la aplicabilidad del sistema biológico anaerobio al tratamiento de aguas residuales conteniendo compuestos orgánicos tóxicos, a las concentraciones utilizadas en la investigación. Sin embargo, la concentración de fenol en el efluente se encontró por encima de 0,5 mg/L, valor exigido por la norma venezolana vigente.
Palabras clave: Reactor UASB, compuestos fenólicos, hidrocarburos saturados.
Introducción
Las aguas residuales producidas en procesos industriales, dependiendo de su procedencia, pueden contener gran cantidad de sustancias orgánicas y/o inorgánicas, en concentraciones que ofrecen peligro para el ambiente. Entre éstas se encuentran fenoles, comunes en la industria fotográfica, fabricación de pinturas, explosivos, caucho, productos farmacéuticos y agrícolas, textiles, curtidoras, papeleras, procesos petroquímicos, etc.; e hidrocarburos saturados, utilizados en la industria como combustibles, lubricantes y disolventes, principalmente [1].
La presencia de estos compuestos en un agua residual, en altas concentraciones, puede limitar la aplicabilidad de algunos sistemas de tratamiento para su depuración, por ejemplo aquéllos que se sirven del metabolismo microbiano para la estabilización de la materia orgánica, debido su efecto inhibidor sobre los microorganismos responsables del tratamiento [2, 3], tal como lo demuestran estudios como el conducido por Leven y col. (2006) [4].
Importantes avances se han logrado en la aplicación de procesos biológicos para la degradación de compuestos fenólicos e hidrocarburos saturados presentes en aguas residuales. Bazaldúa y col. (1996) [5] estudiaron la biodegradación de compuestos fenólicos en un reactor biológico discontinuo secuencial (SBR) adicionado con carbón activado granular; con concentraciones iniciales entre 67-267 mg/L de fenoles totales, los resultados mostraron remociones en compuestos fenólicos superiores al 94%. La biodegradación de compuestos fenólicos presentes en una concentración de 100 mg/L como fenoles totales, de agua preparada en el laboratorio, empleando un reactor anaerobio de lecho fluidizado fue estudiada por Claros y col. (1996) [6], obteniéndose porcentajes de remoción del 97% en la DQO y 99,99% en fenoles totales. Zhao y col. (2000) [7] realizaron estudios de la biodegradación de fenoles en aguas naturales, encontrándose que dicho proceso era posible a la temperatura de mezcla, pH cercano a la neutralidad y alta concentración de oxígeno disuelto. En 2003, Rincón [8] aplicó tratamiento biológico anaerobio usando reactores tipo UASB, a aguas de producción de petróleo liviano, conteniendo 20 mg/L de fenoles totales y 45 mg/L de hidrocarburos totales; en el estudio, con TRH superiores a 10 h y cargas orgánicas inferiores a 2,5 kg DQO/m3 d, se lograron porcentajes de remoción de DQO de hasta 88%. El proceso de degradación de fenoles en aguas de producción petroleras, usando reactores SBR, fue estudiado por Díaz y col. (2004) [9].
Los resultados mostraron que para concentraciones iniciales de 19,16; 1,66 y 2,60 de fenoles totales en aguas de producción de petróleo liviano, mediano y pesado, se obtuvo porcentajes de remoción de 96,8%, 89,2% y 82,8% respectivamente.
El desarrollo de este estudio pretende comprobar la aplicabilidad de un sistema de tratamiento biológico anaeróbico, en la eliminación de fenoles e hidrocarburos saturados presentes en un agua residual preparada en el laboratorio, en
concentraciones iniciales consideradas tóxicas para la biomasa.
Materiales y métodos
Etapas de la investigación
Montaje del reactor UASB. Se utilizó un reactor con capacidad efectiva de 4 litros, acoplado con un cilindro para colectar el biogás producido en el tratamiento. Fue inoculado con 1,2 litros de lodo anaerobio tipo granular, extraído de un reactor del mismo tipo, utilizado para degradar aguas residuales cerveceras. El reactor se montó en uno de los corredores laterales del DISA, operando a temperatura ambiente; las variaciones de temperaturas exteriores estuvieron entre 27°C y 36°C, no hubo necesidad de colocar chaqueta de calentamiento al reactor. Las muestras se preparaban semanalmente y se almacenaban en una cava refrigeradora a 4°C para su conservación antes de su utilización.
Etapa de aclimatación del lodo biológico. El caudal de alimentación del agua residual fue de 2,78 mL/min, correspondiente a un TRH=1d (tiempo de retención hidráulico fijado para el estudio). Luego de cuatro semanas de alimentar el reactor con solución nutriente mostrada en la Tabla 1, se incorporaron los compuestos tóxicos al agua, variando la concentración de cada compuesto fenólico desde 5 hasta 20 mg/L, incrementando a razón de 5 mg/L por cada semana de funcionamiento del reactor, de manera que la biomasa pudiera aclimatarse a su presencia sin sufrir trastornos; los hidrocarburos saturados fueron incorporados al agua residual a la concentración de trabajo (20 mg/L).
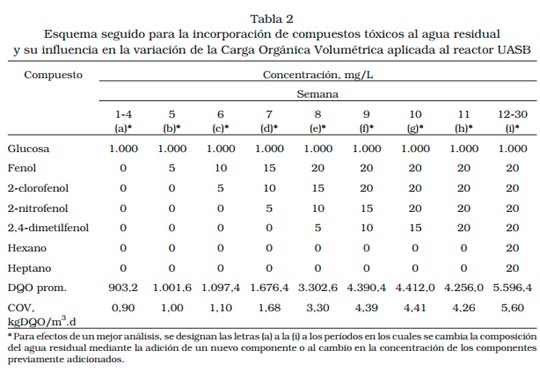
El esquema seguido para la incorporación de los compuestos tóxicos al agua residual, se muestra en la Tabla 2. La etapa de aclimatación se consideró terminada una vez las condiciones del agua a la salida del reactor UASB se mantuvieron relativamente estables (entendiéndose como estabilidad que la remoción de materia orgánica, medida como DQO, permanece constante en 5 días consecutivos), lo cual ocurrió 16 semanas (112 días) después de haberse iniciado la alimentación.
 |
 |
Tratamiento anaerobio del agua residual sintética. Una vez aclimatado el lodo, se continuó la alimentación con el agua residual preparada según la composición nutricional de la Tabla 1 y conteniendo 20 mg/L de cada tóxico mostrado en la Tabla 2. Diariamente se tomaron muestras a la salida del reactor, para monitorear su comportamiento; así mismo se verificó la producción de biogás durante el proceso. La operación del reactor UASB con el lodo aclimatado, comenzó a partir de la semana 17 y se mantuvo hasta las 30 semanas.
Parámetros fisicoquímicos evaluados durante el estudio
Potencial de hidrógeno (pH). Su determinación se llevó a cabo siguiendo la metodología del Standard Methods for the Examination of Water and Wastewater (SM) [10] número 4500-H+ B Método Electrométrico.
Alcalinidad total. Se determinó aplicando el método SM 2320 B Método Titulométrico [10].
Demanda Química de Oxígeno (DQO). Para su determinación se siguió la metodología SM número 5220 C Método Titulométrico, Reflujo Cerrado [10].
Compuestos fenólicos. Su determinación se llevó a cabo aplicando la técnica de cromatografía líquida de alta resolución con sus siglas en inglés HPLC, utilizando un cromatógrafo líquido Hewlett Packard HP 1050, equipado con detector DAD modelo 1100, una columna C18 Hewlett Packard Spherisorb con dimensiones de 125 × 10 mm y 5 µm de diámetro interno. El manejo de los datos se realizó con el software HP ChemStation para LC Rev. A. 06. 01. 403. Como fase móvil se usó una mezcla de Acetonitrilo-IsopropanolAgua en proporción 28,5%:66,5%:5%. Las longitudes de onda óptimas para la lectura de cada fenol fueron: fenol, 270,8 nm y 2-clorofenol, 2-nitrofenol y 2,4-dimetilfenol, 279,8 nm. Se aplicó un flujo isocrático de 0,8 mL/min [11], resultando un tiempo total de corrida de 5,0 min.
Hexano y heptano. Su determinación fue realizada aplicando la técnica de cromatografía de gases, recomendada por el Standard Methods for the Examination of Water and Wastewater, sección 6200, para el análisis de compuestos orgánicos volátiles [10]. Se usó un cromatógrafo Agilent 6890 series GC System, operando bajo las siguientes condiciones: Horno a 40°C por 4 min, isotérmico; Inyector en modo split 10:1, a 200°C; volumen de inyección de 2 µL; Detector de ionización por llama FID a 200°C; Gas de arrastre: helio a 30 mL/min; Columna: HP-5 5% Phenyl Methyl Siloxane Capillary 30,0 m × 320 µm × 0,25 µm nominal; Flujo: 1,8 mL/min (30 cm/s).
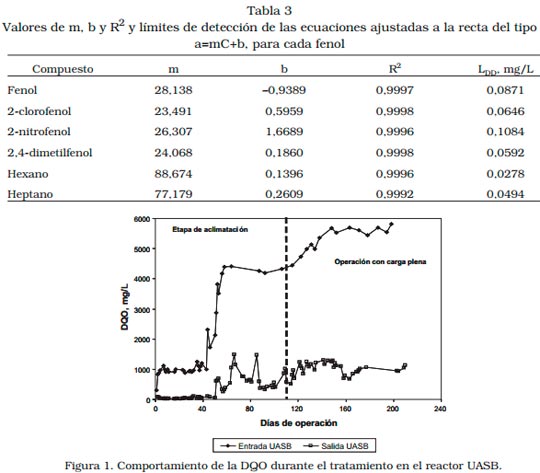
La cuantificación de cada compuesto orgá- nico tóxico se llevó a cabo a través de la calibración haciendo uso de estándares externos, trazando curvas de calibración para cada uno, ajustándolas posteriormente a rectas con ecuaciones de la forma a=mC+b (siendo a el área bajo el pico en el cromatograma y C la concentración del analito). El límite de detección (LDD) se calculó mediante el método de regresión lineal [12]. La Tabla 3 muestra los valores de m, b, R2 , LDD y la ecuación utilizada para cuantificar cada compuesto tóxico.
Porcentaje de metano en el biogás. Fue determinado aplicando la técnica de cromatografía de gases, con la ayuda de un equipo Perkin Elmer Autosystem XL Gas Chromatograph, operando bajo las siguientes condiciones: Horno a 40°C por 15 min, isotérmico; Inyector en modo split 100:1, a 250°C; Volumen de inyección de 200 µL; Detector TCD a 200°C; Gas de arrastre: helio; Columna: Supel Q-Plot Fused Silica Capillary 30,0 m × 0,53 mm i.d.; Flujo: 3,5 mL/min.
Presentación y Discusión de Resultados
Etapa de aclimatación
El objetivo de esta etapa fue adecuar la biomasa del reactor a la presencia de los compuestos orgánicos tóxicos, para de esta manera lograr su biodegradación. El pH del afluente durante la aclimatación se mantuvo entre 7,56-8,32 unidades, mientras que en el efluente presentó valores entre 5,68-7,63 unidades. Se observó una relativa inestabilidad en este parámetro, tanto en el afluente como en el efluente del reactor, durante esta etapa. Por su parte, la Alcalinidad Total del afluente varió entre 360,00-1160,00 mg/L CaCO3, mientras que el efluente presentó valores comprendidos entre 420,00-868,42 mg/L CaCO3.
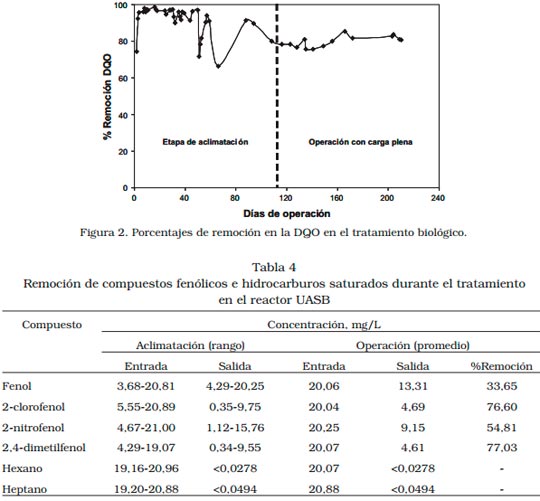
El comportamiento de la DQO en el tratamiento puede observarse en la Figura 1. Durante la aclimatación del lodo biológico, el afluente del reactor UASB presentó valores entre 309,33- 5140,00 mg/L, respondiendo al aumento en la
Carga Orgánica aplicada; en el efluente, la DQO estuvo comprendida entre 10,86-1481,76 mg/L.
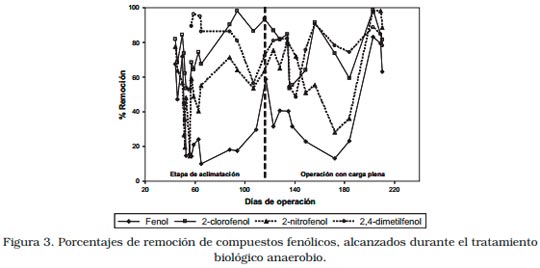
Los porcentajes de remoción en la DQO alcanzados en el tratamiento biológico se ilustran en la Figura 2. En esta Figura puede observarse con claridad la inestabilidad existente en la remoción de la DQO durante la etapa de aclimatación, debido a que durante esta etapa se somete al lodo biológico a constantes incrementos en la Carga Orgánica (con valores comprendidos entre 0,31-5,14 kg DQO/m3 d). Sin embargo, los porcentajes de remoción obtenidos se encuentran, en todos los casos, por encima del 60%.
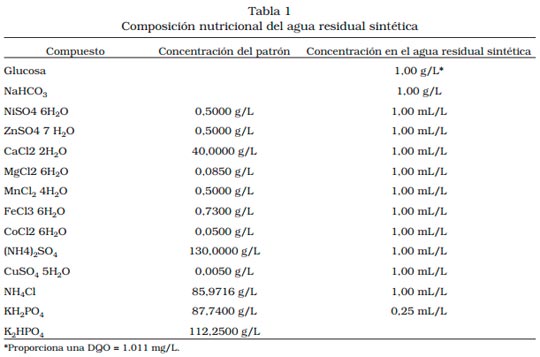
El comportamiento de los fenoles e hidrocarburos saturados durante el tratamiento se resume en la Tabla 4. En esta etapa, se observó una inestabilidad en el comportamiento de los compuestos fenólicos en el efluente del reactor UASB, encontrando por ejemplo, a la salida del reactor, para el 2-nitrofenol concentraciones entre 1,12 mg/L y 15,76 mg/L. Esto se debe a que durante la aclimatación, se varían constantemente las concentraciones de cada compuesto (ver Tabla 2), haciendo variable la respuesta del reactor biológico, en su biodegradación.
Al final de la etapa de aclimatación las concentraciones de los compuestos estuvieron más estables encontrándose así, valores promedios de 14,51 mg/L de fenol, 0,38mg/L de 2-clorofenol, 6,48 mg/L de 2-nitrofenol y 4,56 mg/L de 2,4 dimetilfenol, lo cual permitió considerar esta etapa como culminada. Así mismo, fue posible comprobar la adecuación del lodo para la biodegradación de los compuestos fenólicos e hidrocarburos saturados utilizados en el estudio, a las concentraciones de trabajo, reflejada en la remoción que se logró de cada tóxico por el tratamiento aplicado.
|
|
Etapa de tratamiento del agua residual, conteniendo carga plena de los compuestos orgánicos tóxicos
Luego de finalizada la aclimatación del lodo biológico, se continuó monitoreando el tratamiento del agua residual, conteniendo 20 mg/L de cada compuesto tóxico utilizado.
Durante la operación, el pH presentó un valor promedio de 8,12 ± 0,13 unidades en el afluente y promedió 6,51 ± 0,19 unidades en el efluente del UASB. Se ilustra mayor estabilidad en el pH luego de haberse incorporado todos los tóxicos al agua residual, lo cual provee al lodo biológico mejores condiciones para su operación.
El aumento de la carga orgánica trae como consecuencia una posible acumulación de ácidos grasos en el efluente, esta acumulación podría ser el causante de la disminución del pH con respecto a la entrada. A pesar de esto, el pH se mantuvo dentro del rango recomendado para la digestión anaerobia.
Por su parte, la Alcalinidad presentó los siguientes valores promedio: en el afluente del reactor UASB, 1081,15 ± 136,42 mg/L CaCO3; el efluente, 781,72 ± 118,78 mg/L CaCO3. La Alcalinidad Total fue suficiente para amortiguar los cambios de pH durante el tratamiento, sin comprometer las características del agua residual que permitan su posterior descarga. La DQO tuvo los siguientes valores promedio: 5596,44 ± 143,56 mg/L O2 (correspondiente a una Carga Orgánica aplicada de 5,6 kg DQO/m3 d) en el afluente del reactor UASB; 1033,09 ± 184,65 mg/L O2 en su efluente (Figura 1). El incremento gradual observado en la DQO del afluente se debe a la incorporación de los compuestos orgánicos tóxicos utilizados. La remoción promedio obtenia en la DQO fue de 81,54%, similar a la encontrada por Rincón [8], porcentaje bastante elevado para este tipo de proceso, considerando las características
del agua residual tratada (Figura 2).
Con respecto a los compuestos fenólicos e hidrocarburos saturados, el comportamiento observado se resume en la Tabla 4, alcanzándose con el tratamiento los siguientes porcentajes de remoción para cada uno de ellos: fenol, 33,65%; 2-clorofenol, 76,60%; 2-nitrofenol, 54,81% y 2,4-dimetilfenol, 77,03%. Al igual que durante la etapa de aclimatación, las concentraciones de hexano y heptano estuvieron por debajo de 0,0278 mg/L y 0,0494 mg/L respectivamente, el cual corresponde a los límites de detección de dichos compuestos. Su eliminación del agua residual a su paso por el reactor puede deberse posiblemente a la biodegradación durante el tratamiento biológico, así como también al proceso de volatilización de estos compuestos durante el proceso, dado su bajo punto de volatilización, el cual no fue evaluado. Tampoco se evaluó el proceso de adsorción de los compuestos estudiados en el lodo biológico, cuya influencia no se descarta.
En la Figura 3 se ilustran los porcentajes de remoción para cada compuesto fenólico utilizado, durante el tratamiento biológico. En esta Figura se puede observar cómo, al incrementarse la concentración de los compuestos 2-clorofenol,
2-nitrofenol y 2,4-dimetilfenol en el agua residual, el porcentaje de remoción del fenol sufre una caída, siendo el menor entre los cuatro compuestos fenólicos utilizados. Se observa además que hacia el final del tratamiento existe un importante incremento en la remoción de todos los fenoles, alcanzando valores superiores al 80%.
Análisis del biogás producido en el reactor biológico
El análisis de la mezcla de gases conocida como biogás, producido durante el tratamiento biológico anaerobio, se toma como una medida del funcionamiento del reactor. Para esto, se de termina el porcentaje de metano contenido en el biogás, debido a que este compuesto es producto principal en este tipo de tratamiento. En la Figura 4 se ilustra la producción de biogás en el reactor UASB, durante el tratamiento. El aumento observado en la producción de biogás en el reactor UASB, se debe al aumento en la Carga Orgá- nica aplicada y su posterior biodegradación. Al analizar cromatográficamente el biogás producido en el tratamiento del agua residual utilizada en el estudio, se encontró en él un porcentaje de metano de alrededor del 65%, valor que verifica que en el reactor UASB se lleva a cabo el proceso de biodegradación de la materia orgánica, representada en este caso por glucosa, compuestos fenólicos e hidrocarburos saturados, lo cual hace inferir que los procesos de adsorción en lodos o volatilización de los compuestos orgánicos incorporados al reactor, no son los mecanismos de eliminación que prevalecen en este estudio. Diversos estudios han demostrado la posible degradación por vía biológica de hidrocarburos alifáticos de cadena corta. Vieth y Wilkes [13], utilizando isótopos estables en estudios a escala de laboratorio, cuantificaron la pérdida de n-hexano por biodegradación. Rahman y col. [14], encontraron una degradación completa de n-alcanos de nC8–nC11, después de 56 días de biorremediación en lodos petrolizados provenientes de fondos de tanques de crudo.
|
|
Conclusiones
Es posible la aclimatación del lodo biológico anaerobio para la degradación de sustancias orgánicas, consideradas tóxicas para la biomasa, a las concentraciones utilizadas en esta investigación.
Los porcentajes de remoción promedio logrados por el tratamiento biológico anaerobio fueron: 81,54% en la DQO; 33,65% para el fenol; 76,60% para el 2-clorofenol; 54,81% para el 2-nitrofenol y 77,03% para el 2,4-dimetilfenol.
Los compuestos hexano y heptano estuvieron por debajo de 0,0278 mg/L y 0,0494 mg/L respectivamente, el cual corresponde a los límites de detección de dichos compuestos utilizando la técnica de cromatografía gaseosa.
La eficiencia del tratamiento aplicado para la remoción de fenoles e hidrocarburos saturados, está sujeta a las condiciones de operación aplicadas.
El tratamiento del agua residual en el reactor UASB, con un tiempo de retención hidráulico de 24 horas, no logró una remoción satisfactoria de los compuestos fenólicos ni de la DQO, por lo cual se requiere la aplicación de un tratamiento posterior que permita alcanzar concentraciones en el efluente, menores a las permitidas por la legislación ambiental venezolana vigente, para la descarga a cuerpos de aguas naturales.
Agradecimientos
Los autores expresan su agradecimiento al Fondo Nacional de la Ciencia y la Tecnología (FONACIT) y al Consejo de Desarrollo Científico y Humanístico (CONDES) por el financiamiento de este proyecto.
Referencias Bibliográficas
- Organización Internacional del Trabajo-OIT. Enciclopedia de salud y seguridad en el trabajo. Ministerio de Trabajo y Asuntos Sociales. Subdirección General de Publicaciones, 1998.
- Ingraham, J.; Ingraham, C. Introducción a la Microbiología. Editorial Reverté S.A. España, 1994.
- Madigan, Martinko, Parker. Brock. Biología de los microorganismos. Octava edición revisada. Prentice Hall. Madrid, España, 1999.
- Leven L., Nyberg K., Konkea-Aho L., Schnurer A. Phenols in anaerobic digestion processes and inhibition of ammonia oxidizing bacteria (AOB) in soil. The science of the total environment. Vol. 364, (2006) 1-3.
- Bazaldúa R, García L., Buitrón G. Operación de un proceso discontinuo secuencial (SBR) adicionado con carbón activado granular para la biodegradación de compuestos fenólicos. Coordinación de Bioprocesos Ambientales, Instituto de Ingeniería. Universidad Nacional Autónoma de México, C.U. México (1996).Disponible en: http://www.cepis. ops-oms.org/eswww/fulltext
- Claros C., Acosta A., Stia E., Delfino J., Higa L. Biodegradación de compuestos fenólicos empleando un reactor anaeróbico de lecho fluidizado a escala piloto. Instituto Nacional de Ciencia y Técnica Hídricas-Centro de Tecnología del Uso del Agua y el Ambiente. Argentina (1996). Disponible en: http:// www.cepis.ops-oms.org/eswww/fulltext
- Zhao J., Zhang K., Li C., Luo P. Study on biodegradation of phenols in river water. Journal of West China University of Medical Sciences. Vol. 31, No. 3 (2000) 367.
- Rincón Lizardo, N. Tratamiento anaerobio de las aguas de producción de petróleo liviano. Trabajo de Ascenso para la categoría de Profesor Asociado. Departamento de Ciencias Naturales. Programa de Ingeniería Civil. La Universidad del Zulia. Venezuela (2003). Pp.150.
- Altamira Díaz, Nancy Rincón, Julio Marín, Elisabeth Behling, Elsa Chacín y Nola Fernández. Degradación de fenoles durante el tratamiento biológico de aguas de producción petroleras. Ciencia, Vol. 13 No. 4 (2005) 281-291.
- APHA. AWWA. WPCF. Standard Methods for the Examination of Water and Wastewater. 20th Edition, 1998.
- Zhao L, Lee H. J. Determination of phenols in water using liquid phase microextraction with back extraction combined with high-performance liquid chromatography. Journal of Chromatography A. Vol. 931 (2001), 95-105.
- Miller, J.; Miller, J. Estadística para Química Analítica. Segunda Edición. México D.F., México. Ed. Addison-Wesley Iberoamericana, 2001.
- Vieth A. and Wilkes H. Deciphering biodegradation effects on light hydrocarbons in crude oils using their stable carbon isotopic composition: A case study from the Gullfaks oil field, offshore Norway. Geochimica et Cosmochimica Acta. Vol. 70 No. 3 (2006), 651-665.
- Rahman K.S.M., Rahman T., Kourkoutas Y., Petsas I., Marchant R., Banat I.M. Enhanced bioremediation of n-alkane in petroleum sludge using bacterial consortium amended with rhamnolipid and micronutrients. Bioresource Technology Vol. 90 (2003) 159-168.
Autores: Víctor Vacca J., Nancy Rincón*, Gilberto Colina, Julio Marín, Altamira Díaz, Elisabeth Behling, Elsa Chacín y Nola Fernández
Departamento de Ingeniería Sanitaria y Ambiental (DISA), Escuela de Ingeniería Civil,
Facultad de Ingeniería, Universidad del Zulia, Apartado 526. Maracaibo 4001-A, Venezuela
Fuente: www.scielo.org.ve