Purificación y acondicionamiento del gas de gasificación de biomasa
Resumen
En el proceso de gasificación de biomasa se obtiene un gas susceptible de utilización en calderas, motores, turbina de gas y turbina de vapor (ciclo combinado), pilas de combustible y síntesis química. No obstante, es necesaria una etapa previa de depuración y acondicionamiento del mismo con objeto de eliminar contaminantes a niveles suficientemente bajos para cumplir con la normativa medioambiental y la tolerancia de los sistemas de conversión del gas, ajustar la relación CO/H2 y mejorar la calidad del gas previo a su aprovechamiento energético o a su conversión en combustibles limpios (H2 y combustibles sintéticos, etc.) y contribuir a la reducción progresiva de emisiones responsables de la acidificación (NH3 ) y del efecto invernadero (CO2 , CH4 ). La presente contribución pretende ofrecer una visión general y divulgativa sobre las diferentes tecnologías de depuración y acondicionamiento del gas de gasificación de biomasa disponibles actualmente, con indicación de su grado de desarrollo.
1. Utilización del gas de gasificación de biomasa
Tanto el tipo de proceso de gasificación, como los requerimientos a cumplir para las distintas aplicaciones finales condicionarán el sistema de limpieza y acondicionamiento del gas a utilizar [1-4]. Cuando la biomasa u otro combustible se somete a gasificación se obtiene un gas formado mayoritariamente por CO, H2 , CH4 , H2 O, N2 y CO2 .
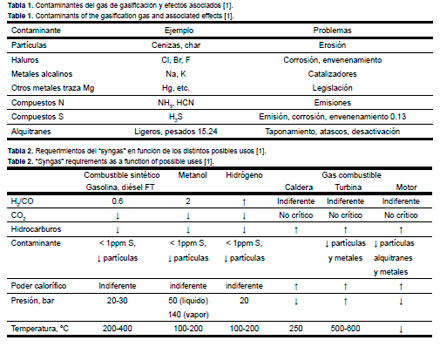 |
La composición del gas dependerá del tipo de reactor (lecho móvil en co-corriente o contracorriente, lecho fluidizado burbujeante o circulante, lecho arrastrado), de las condiciones de operación (presión y temperatura) y de la naturaleza del agente gasificante (aire, oxígeno, vapor, hidrógeno o alguna de sus mezclas) [1, 2, 5], pudiéndose encontrar los siguientes usos potenciales: generación de calor en una caldera o en un motor, generación de calor y electricidad en una turbina de gas y en una turbina de vapor (ciclo combinado), generación eléctrica en una pila de combustible y síntesis química de metanol, gas natural sintético, hidrógeno, combustibles sintéticos vía Fischer Tropsch, etc. [1].
Durante la gasificación se forman a su vez otras impurezas no deseadas [1, 3, 4]. En la tabla 1 se han resumido los principales contaminantes y los problemas potenciales asociados a los mismos. Generalmente, la composición del gas (“syngas”) a la salida del gasificador no es la más adecuada para su uso final. En la tabla 2 se recogen las características deseables del “syngas” para diferentes aplicaciones [1, 3-5].
2. Depuración y acondicionamiento del gas de gasificación.
De acuerdo a lo anterior, previo a la utilización del “syngas” será necesaria la depuración y acondicionamiento del mismo con objeto de: eliminar contaminantes a niveles suficientemente bajos para cumplir con la normativa medioambiental y la tolerancia de los sistemas de conversión del gas, ajustar la relación CO/H2 y mejorar la calidad del gas previo a su aprovechamiento energético o a su conversión en combustibles limpios (H2 , síntesis química) y contribuir a la reducción progresiva de emisiones responsables de la acidificación (NH3 ) y del efecto invernadero (CO2 , CH4 ) [3, 6-8].
La limpieza de los gases se ha realizado tradicionalmente por vía húmeda, lo que implica el enfriamiento de los gases a temperatura ambiente o inferior, con lo que la generación de vapor en turbina de gas es menos eficiente. Además, conlleva unos costes tremendamente elevados y la generación de un gran volumen de efluentes a tratar por métodos costosos [3]. Pese a ello se emplea en la mayoria de las plantas de gasificación existentes, en especial para aplicaciones del gas a baja temperatura, al considerarse una tecnología madura, con eficacia contrastada y de fácil diseño y aplicación a cada sistema particular [3]. Sin embargo, la limpieza de los gases en caliente (T>300ºC) permite una mayor integración con los sistemas catalíticos de ajuste de la composición del gas posteriores, un mejor balance energético y una mejor economía del proceso, al tiempo que se eliminan los problemas derivados de la gestión de efluentes [3].
3. Limpieza de gases a baja temperatura.
Habitualmente el gas que sale del gasificador sufre una etapa de separación de partículas groseras en un ciclón. A continuación tienen lugar una serie de etapas que constituyen la limpieza a baja temperatura y que incluye un lavado con agua y la eliminación de los gases ácidos [3]. Durante la etapa de lavado con agua las partículas, los alquitranes,NH3 , HCN y haluros son eliminados de la corriente gaseosa [3-6]. Se eliminan también elementos traza a 100-200o C por condensación [6]. Así mismo, se han desarrollado métodos alternativos de eliminación de alquitranes en torres de lavado con disolventes orgánicos en combinación con filtro de pre-capa [9] o precipitador húmedo [10], previo a utilización del gas en calderas y motores. Finalmente es necesaria una etapa de purificación del gas para eliminación de gases ácidos (H2 S y/o CO2 ) por absorción, previo a su uso en turbinas de gas o pilas de combustible [3, 4]. Con vistas a reducir las emisiones de gases de efecto invernadero, todo el CO se convierte previamente a CO2 por vía catalítica (reacción de gas de agua: CO + H2 O ↔ CO2 + H2 ), aunque la penalización energética es severa [6]. La absorción se lleva a cabo en columnas de relleno, torres de pulverización o tanques agitados en contracorriente utilizando disoluciones acuosas alcalinas de componentes orgánicos e inorgánicos. El absorbente es regenerado en una columna contigua, recuperándose el contaminante en su forma inicial. La absorción puede ser física (Procesos Rectisol, Purisol y Selexol), o química (aminas orgánicas, carbonatos de sodio y potasio y disoluciones acuosas de amoníaco) [2, 6]. La adsorción, la separación criogénica y la tecnología de membranas también pueden emplearse como alternativas a la absorción en la separación de gases ácidos a bajas temperaturas [6].
4. Limpieza de gases a alta temperatura.
En la primera etapa de eliminación de partículas, la tendencia es a aumentar la temperatura de operación y a reducir la concentración y tamaño de partícula (por debajo de 10 ppm en peso y de 2 micras) mediante el desarrollo de diferentes sistemas de filtración: candelas cerámicas, filtros cerámicos de flujo cruzado, precipitadores electrostáticos de alta temperatura y presión, filtros de lechos granulares y filtros de tejido/fibra [2, 3, 5-7]. La eliminación de compuestos de azufre (H2 S y COS) se lleva a cabo por adsorción. El sólido adsorbente puede inyectarse en el propio gasificador a 800-1000ºC, pero no puede ser reutilizado, lo que le obliga a ser abundante y barato (caliza, dolomita, etc.), generándose una gran cantidad de residuos cuyo manejo implica un elevado consumo energético. En la práctica, la eficacia de retención de azufre no supera el 50% dependiendo de la temperatura y velocidad de calcinación [5]. Debido a estas limitaciones se han desarrollado adsorbentes (mayoritariamente óxidos de hierro y zinc) y sistemas de desulfurización en lechos externos al gasificador. El óxido metálico debe reaccionar selectivamente (MO(s) +H2 S → MS(s) + H2 O) con los compuestos de azufre en atmósfera reductora y en las condiciones habituales de salida de un gasificador (P=10-30 bar, T= 500-750ºC), pudiendo ser de un sólo uso (baratos) o regenerables (caros) [2, 3, 6-8]. Los adsorbentes regenerables deben recuperar su forma original al reaccionar selectivamente con oxígeno o vapor (MS +3/2 O2 → MO + SO2 ), siendo necesario controlar la temperatura de regeneración (exotérmica) para evitar la sinterización del adsorbente [3, 6-8]. La naturaleza cíclica del proceso adsorciónregeneración obliga a una configuración de dos reactores operando en continuo. Inicialmente se emplearon lechos fijos, actualmente se tiende hacia los lechos fluidizados debido a su mejor contacto gas-sólido, aunque con mayor atrición [6-8]. Entre las tecnologías para la eliminación deNH3 y HCN se encuentra la descomposición catalítica (sobre Ni, Fe,..) a unos 800ºC [3, 5, 6-8]. También se está investigando la eliminación simultánea deNH3 y H2 S mediante adsorbentes duales de níquel y titanato de zinc [7, 8]. En cuanto a los haluros, la tendencia actual es a emplear adsorbentes de metales alcalinos o alcalinotérreos [3, 6-8]. En relación a los álcalis, se eliminan con adsorbentes multifuncionales (aluminosilicatos impregnados con calcio) [3, 6-8]. El empleo combinado de filtros cerámicos y adsorbentes o catalizadores (a 400-600 ºC) permite la eliminación conjunta de partículas, alcalis y haluros [5]. También se utilizan tecnologías de eliminación en caliente de metales pesados no condensados (incluyendo Pb, Hg, Cd, V), principalmente por adsorción [3, 6, 8]. En el caso concreto del Hg se están desarrollando carbones activos selectivos [3] con etapas previas de oxidación forzada del Hgº (no se retiene) por vía química o electroquímica. Por último, la eliminación de los alquitranes a alta temperatura se basa en su separación física (en sistemas de eliminación de partículas) [3] o en su conversión química (craqueo, reformado, oxidación, etc.) por vía termica y/o catalítica [2, 4, 5, 7, 11-15]. El craqueo térmico consiste en la transformación del alquitrán en gases ligeros mediante calentamiento a una temperatura determinada (500-1200ºC) durante un cierto tiempo (0.5-15 s) [4, 13]. La eficacia se puede mejorar aumentando el tiempo de residencia (lechos fluidizados) o la temperatura (por contacto directo u oxidación parcial), con el consiguiente incremento del gasto energético y pérdida de poder calorífico, respectivamente [4]. A los problemas económicos y de materiales hay que añadir aquellos asociados con la potencial formación de carbonilla [5, 14]. Otra posible vía se basa en el craqueo térmico mediante plasma, que, aun siendo sistemas muy novedosos y efectivos, presentan un elevado coste económico y energético [4, 13, 14]. En cuanto a la vía catalítica, el catalizador debe ser [13, 14]: efectivo, capaz de reformar metano (en su caso a gas de síntesis), resistente a la desactivación por sinterización y carbonilla, fácilmente regenerable y tener un coste moderado. El agente catalítico se puede alimentar al propio reactor (gasificación o pirólisis catalítica) [4, 11, 12] o a un reactor secundario para tratar el gas bruto de gasificación [5]. Se distinguen seis grupos de catalizadores: de base Ni, de base metálica (Rh, Ru, Pd, Pt Ir, Co, Fe, Mo y La), metales alcalinos (K2 CO3 , NaCl, LiCl, KCl, etc.), básicos (MgO, CaO, dolomita, olivino, etc.), ácidos (zeolitas y aluminosilicatos) y carbones activados (o incluso char de gasificación) [4, 5, 13-16].
5. Ajuste de la composición del gas y síntesis química.
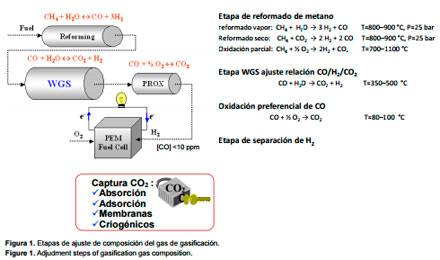
Además de eliminar las impurezas del gas de gasificación, es necesario someterlo a un conjunto de etapas de ajuste de su composición en función del uso final al que se destine (Figura 1) [16-19]. La primera etapa es el reformado con vapor de agua o seco (con CO2 ) o una combinación de ambos o la oxidación parcial de CH4 u otros hidrocarburos ligeros para reducir su contenido en el gas por debajo del 0.5-1% e incrementar el de H2 [4, 18, 19]. Se utilizan catalizadores, principalmente de base Ni, a temperaturas inferiores a 1000ºC [18]. Le sigue una etapa de “water gas shift” para ajuste de la relación CO/H2 /CO2 previo a la sintesis química o separación de H2 [19]. Industrialmente se realiza en dos reactores catalíticos adiabáticos en serie, con enfriamiento intermedio, operando entre 320-360ºC y 190-250ºC, respectivamente. A alta temperatura se distingue entre catalizadores dulces (óxidos mixtos de Fe/Cr o sustituidos parcialmente por Ag, Ba, Pb ó Hg/Cu, Ca, Ce, Zr, La, Th,.., Pt, Rh, Ru, Au, y Pd sobre óxidos reducibles), para los que es necesario retirar previamente el azufre y ácidos (Co-Mo, Co-MnO y CoCr2 O4 ) que operan con azufre pero a un coste mayor. La conversión de CO es normalmente superior al 90%, desactivándose principalmente
 |
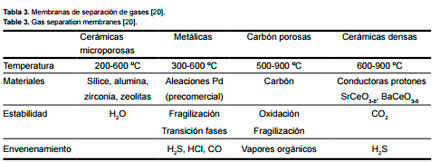 |
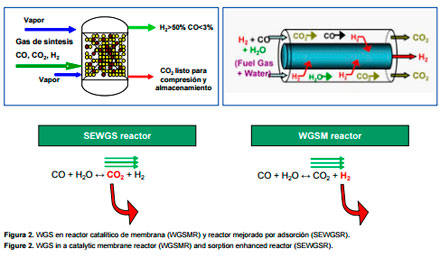
por sinterización térmica [19]. Los catalizadores de baja temperatura se basan principalmente en CuZnO-Al2 O3 /Cr2 O3 . Se siguen estudiando métodos de preparación, naturaleza de precursores y mecanismos de reacción, para mejora de la actividad catalítica a baja temperatura, efecto del tiempo de residencia y relación vapor a gas y tolerancia a azufre y cloro, así como el desarrollo de catalizadores alternativos (espinelas de Cu y Mn, Au o Au/Ru sobre óxidos reducibles, etc.), de nuevas configuraciones de reactor (monolitos) y la intensificación de procesos (reactores de membrana, de adsorción mejorada o combinación ambos) [17, 19]. Cuando el H2 va a ser utilizado en pilas de combustible poliméricas (PEM) es necesaria además una etapa posterior de oxidación preferencial de CO para evitar el deterioro de la membrana [18]. La producción de H2 a partir de la corriente de salida de la etapa “shift” se lleva a cabo por separación de éste, o por separación de CO2 y posterior purificación de la corriente rica en H2 [17, 18]. Comercialmente el CO2 se separa por absorción (química o física), seguida de purificación por adsorción en ciclos de presión (PSA), adsorbiéndose los componentes indeseados (CO, CO2 ) a alta presión, y liberándose posteriormente, regenerando el adsorbente, por despresurización [17, 18]. En fase de investigación y desarrollo se encuentra la tecnología de membranas para obtención de H2 de alta pureza [20]. En la tabla 3 se resumen los tipos de membranas de separación y sus caracteristicas [20]. Dentro del concepto de integración de sistemas están los reactores catalíticos de membrana y/o de adsorción mejorada (Figura 2), que permiten separar simultáanea y selectivamente el H2 , el CO2 o ambos del medio de reacción y desplazar el equilibrio hacia los productos [17, 18]. Finalmente, la síntesis química comprende un conjunto de procesos que permiten la conversión en combustibles (diesel y gasolina vía Fischer-Tropsch, metano, metanol, etanol, dimetiléter, etc.) del CO e H2 contenidos en el gas de síntesis [1-5]. La relación H2 /CO deseable, las condiciones de operación y los catalizadores utilizados dependen del producto final [2].
6. Bibliografía
[1] Ciferno JP, Marano JJ, US Department of Energy NETL. Benchmarking Biomass Gasfication Technologies for Fuels, Chemicals and Hydrogen Production, 2002.
[2] Held J, Swedish Gas Centre. Gasification – Status and technology (Rapport SGC 240 • 1102-7371 • ISRN SGC-R- 240-SE) Ed.: Swedish Gas Centre, 2012.
[3] Woolcock P, Brown RC. A review of cleaning technologies for biomass-derived syngas. Biomass and Bioenergy 2013; 52:54–84.
[4] Basu P. Chapter 9-Production of Synthetic Fuels and Chemicals from Biomass. In: Prabir Basu Eds. Biomass Gasification and Pyrolysis Practical Design and Theory. Elsevier, Inc. 2010 p. 301-323.
[5] Kumar A, Jones DD, Hanna MA. Thermochemical Biomass Gasification: A Review of the Current Status of the Technology. Energies 2009; 2:556–581.
[6] Thambimuthu KV, IEA Coal Research. Clean Coal Centre. Gas Cleaning for advanced coal-based power generation. (IEACR/53) Ed.: International Energy Agency Coal Research, 1993.
[7] Mitchell SC, IEA Coal Research. Clean Coal Centre. Hot gas cleanup of sulphur, nitrogen minor and trace elements. (CCC/12) Ed.: International Energy Agency Coal Research, 1998.
[8] Williams BC, McMullan JT, University of Ulster. Hot Gas chemical clean-up: current commercial and technological status. (ETSU-COAL-R-139) Ed.: Harwell Laboratory, Coal R & D Programme, 1998.
[9] Hofbauer H, Rauch R, Bosch K, Koch R, Aichernig C. Biomass CHP Plant Güssing – A Success Story. Expert Meeting on Pyrolysis and Gasification of Biomass and Waste. Strasbourg, Octubre 2002.
[10] Zwart RWR, Van der Drift A, Bos A, Visser HJM, Cieplik MK, Könemann HWJ. Oil-based gas washing-Flexible tar removal for high-efficient production of clean heat and power as well as sustainable fuels and chemicals. Environmental Progress & Sustainable Energy 2009; 28(3):324–335.
[11] Devi L, Ptasinski KJ, Janssen FJJG. A review of the primary measures for tar elimination in biomass gasication processes. Biomass and Bioenergy 2003; 24:125–140.
[12] Sutton D, Kelleher B, Ross JRH. Review of literature on catalysts for biomass gasification. Fuel Processing Technology 2001; 73:155–173.
[13] Samsudin A, Zainal ZA. Tar reduction in biomass producer gas via mechanical, catalytic and thermal methods: A review. Renewable and Sustainable Energy Reviews 2011; 15(5):2355–2377.
[14] Han J, Kim H. The reduction and control technology of tar during biomass gasification/pyrolysis: An overview. Renewable and Sustainable Energy Reviews 2008; 12(2):397–416.
[15] Shen Y, Yoshikawa K. Recent progresses in catalytic tar elimination during biomass gasification or pyrolysis—A review. Renewable and Sustainable Energy Reviews 2013; 21:371–392.
[16] Richardson Y, Blin J, Julbe A. A short overview on purification and conditioning of syngas produced by biomass gasification: Catalytic strategies, process intensification and new concepts. Progress in Energy and Combustion Science 2012; 38:765–781.
[17] DOE/NETL. Advanced Carbon Dioxide Capture R&D Program: Technology Update, May 2013 Appendix B: Carbon Dioxide Capture Technology Sheets. National Energy Technology Laboratory. U.S. Department of Energy. http://www.netl.doe.gov/File%20Library/Research/Coal/ carbon%20capture/handbook/CO2-Capture-Tech-Update- 2013-Appendix-B.pdf
[18] Harrison DP. Sorption-Enhanced Hydrogen Production: A Review. Industrial & engineering chemistry research 2008; 47(17): 6486–6501.
[19] Ratnasamy C, Wagner JP. Water Gas Shift Catalysis. Catalysis Reviews: Science and Engineering 2009; 51(3):325–440.
[20] Gallucci S, Fernandez E, Corengia P, Van Sint Annaland M. Recent advances on membranes and membrane reactors for hydrogen production. Chemical Engineering Science 2013; 92:40–66.
 |
Por: E. Ruiz, J.M. Sánchez
Fuente: www.gecarbon.org