| Este reporte lo familiarizará con los problemas envueltos en la selección de un sistema de adsorción para su planta, compañía o corporación. Cada uno de los adsorbentes de carbón, zeolitas y polímeros, han sido utilizados para adsorber compuestos orgánicos volátiles (COV) y otros contaminantes en el aire, a concentraciones relativamente diluídas (de decenas a miles de partes por millón por volumen), para controlar emisiones.
Este reporte discute los problemas relacionados con decidir cuál adsorbente se va a utilizar, que tipo de sistema de adsorción seleccionar, y qué tecnología de control de emisión es correcta para su caso. |
| |
|
¿Qué son los sistemas de adsorción?
|
| |
| Nos referimos a los sistemas con adsorbentes, no con absorbentes, porque el contaminante es adsorbido sobre la superficie (principalmente por la superficie interna) de un gránulo, perla o cristal de material adsorbente. No es absorbido por medio de reacción química. Esta es una diferencia importante. El material adsorbido es retenido físicamente sin demasiada fuerza y puede ser liberado (desorbido) de modo relativamente fácil ya sea por calor o al vacío. Por el contrario, un absorbente reacciona químicamente con la sustancia que está siendo absorbida y de esta manera retiene la sustancia absorbida mucho más fuertemente, requiriendo mucha más energía para liberarla.
Desafortunadamente, uno de los adsorbentes es llamado “carbón absorbente”. Esta persistente confusión proviene de antes de los años veinte, cuando la adsorción llegó a entenderse. Un término más apropiado es el de “carbón activado”. El carbón se activa por medio de la pirólisis del carbón mineral, la madera, la corteza de árbol, la cáscara del coco, etc., para eliminar todo el material volátil en forma de gas o vapor y dejar únicamente el carbón elemental. A continuación, este carbón también podría ser parcialmente oxidado para agrandar sus poros.
Otro adsorbente es la estructura cristalina de aluminosilicato conocida como “zeolita”, que posee poros de tamaño uniforme (también llamados ventanas), a través de toda su estructura de cristal. La estructura de cristal de los 118 tipos establecidos de zeolitas se determina por la relación de silicio a aluminio en el cristal cuando este cristal se forma. Toda la zeolita que ocurre naturalmente es hidrofílica (o sea, que posee una afinidad por las moléculas polares, tales como el agua) y contiene aluminio. La desaluminización de la zeolita natural la vuelve hidrofóbica (o sea, que posee afinidad por las sustancias no polares, tales como muchos COV). Las zeolitas se desaluminizan por medio del intercambio del aluminio por silicio sin cambiar la estructura del cristal.
La zeolita hidrofóbica también puede ser sintetizada en cristales desde 1 micra hasta 1 milímetro de diámetro y éstos pueden ser aglomerados en forma de gránulos más grandes y reducir su resistencia al flujo del aire. Puesto que la síntesis es costosa, por lo general se reserva para producir ya sea las zeolitas hidrofóbicas o catalizadores de zeolita con un tamaño específico de poro grande.
Los polímeros adsorbentes poseen poros formados durante su manufactura. Estos poros pueden variar desde macroporos hasta tamaños moleculares, pero los poros más pequeños son por lo general más grandes que los microporos de un carbón activado. Los polímeros se utilizan como gránulos o perlas y, como el nombre lo implica, son plásticos. Se ha observado que desorben más rapidamente que el carbón. Al igual que el carbón, no son considerados altamente selectivos con respecto a cuál COV van a adsorber, aunque cualquier polímero específico adsorberá a algunos COV mejor que a otros.
La selección del mejor adsorbente para cada situación no es sencilla. Hay varios problemas relacionados que discutiremos para familiarizarlo con los diferentes adsorbentes y sistemas. |
| |
|
¿Por qué son importantes los sistemas de adsorción?
|
| |
| Los sistemas de adsorción han sido utilizados principalmente para controlar la emisión de COV. Típicamente, el control de emisiones de COV reduce las concentraciones desde un rango entre 400 y 2,000 partes por millón (ppm) hasta menos de 50 ppm. Actualmente, la tecnología de adsorción puede ampliar este rango de concentración de COV desde 20 ppm hasta una cuarta parte del Límite Inferior de Explosividad (LIE). En el extremo inferior de este rango, las concentraciones tan bajas pueden ser difíciles o muy caras como para ser controladas por alguna otra tecnología y ni por todos los adsorbentes. En el extremo superior del rango de concentraciones, los incineradores, los separadores por membrana y los condensadores, pueden ser económicamente viables cuando son utilizados en lugar de los sistemas de adsorción.
Además del control de emisión, un sistema de adsorción hace posible la recuperación de COV. La recuperación de un COV reutilizable o comercial puede contrarrestar significativamente el costo de controlar la emisión. Los sistemas de adsorción también pueden aumentar la concentración de COV, permitiendo que la destrucción por incineración o la recuperación por membrana o por condensador sean económicamente viables. |
| |
|
¿Cómo funciona la adsorción?
|
| |
Los COV son vapores condensables que parecen condensarse sobre la superficie del adsorbente. Cuando la superficie ha adsorbido casi todo lo que le es posible, el COV es desorbido como parte de la regeneración del adsorbente. Por lo general, al ser desorbidos, los vapores de COV se encuentran a una concentración más alta, después de lo cual el COV puede ser recuperado o destruido. Se podría generalizar que la función de todos los sistemas de adsorción es la captura de COV a partir de una concentración diluída y su liberación a una concentración más alta. Los sistemas de adsorción también pueden ser considerados como separadores del flujo de COV y del flujo de aire de un proceso.
La concentración real del COV es la clave para determinar cúando y cómo se va a utilizar un sistema de adsorción. Un sistema de adsorción se vuelve casi inútil cuando la concentración a la entrada disminuye tanto que el COV no será adsorbido efectivamente, pero permite que la recuperación del COV sea a una concentración alta. Por razones de seguridad se indica que las concentraciones de COV se mantengan por debajo de la cuarta parte del LIE. Cuando la concentración está cerca de una cuarta parte del LIE, se puede disponer económicamente del COV por medio de un incinerador, capturar por una membrana, o recuperar con un condensador. Sin embargo, una concentración por debajo de una cuarta parte del LIE es demasiado baja para sustentar la combustión sin añadir un combustible auxiliar. Por lo tanto, a medida que la concentración de COV a la salida del adsorbente desciende por debajo de una cuarte parte del LIE, se debe añadir más combustible para proporcionar una combustión adecuada al COV en un incinerador. |
| |
|
¿Cómo son adsorbidos los cantaminantes?
|
| |
En la figura 1 se muestra una molécula sobre una superficie, a la distancia a la que normalmente se encuentra de dicha superficie. Existe una repulsión entre la nube de electrones en los átomos que forman la superficie y los de la molécula y existe además una fuerza de atracción nuclear de Van der Waals. La atracción nuclear tiene un radio de influencia mucho más corto, de manera que hay una distancia corta ( por lo general de nanómetros), desde la superficie, donde existe un “vado” o “pozo” en la curva de energía potencial tal como se muestra en la figura 2. Las moléculas o los átomos que llegan a este “pozo”, son atrapados o “adsorbidos” por este “pozo” de energía potencial hasta que pueden obtener la suficiente energía cinética para escapar fuera del pozo. La energía cinética se convierte en energía potencial, tal como cuando uno brinca hacia arriba en contra de la gravedad. Por lo tanto, se debe añadir energía cinética para permitir que las molécula escapen o se “desorban”. La energía cinética de las moléculas se manifiesta como temperatura; siendo más energética cuanto más caliente.
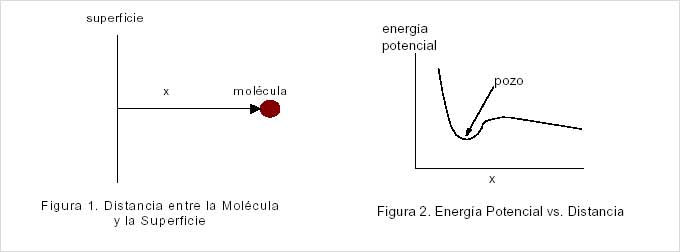 |
|
| Históricamente, el carbón fue el primer material en el que se observó que contenía una gran superficie con esta propiedad. Más recientemente, se ha observado que los adsorbentes de zeolita y de polímeros también poseen una gran superficie interna con esta propiedad.
Durante décadas hemos sabido que antes de poder obtener un alto vacío (tal como 1 micra de Hg), aún los sistemas de vidrio deben “desgasar” el aire adsorbido. Lo que distingue a estos adsorbentes, es que tienen una superficie tan grande (principalmente interna), con esta propiedad por unidad de peso y que puede ser desorbida sin dificultad. |
|
|
|
¿Qué es la desorción?
|
| |
| La desorción se logra a través de oscilaciones tanto de temperatura como de presión. De acuerdo a la teoría cinética de la materia, las moléculas ganan energía cinética cuando son calentadas y ésto permite que una molécula calentada “vuele” fuera del pozo. El calor puede ser proporcionado por medio de vapor, nitrógeno calentado o por microondas, entre otras técnicas. Para la regeneración al vacío, la molécula tendrá en algún momento suficiente energía como para escapar, siempre que los choques entre las moleculas no la envíen de nuevo hacia el pozo. Por lo tanto, la desorción puede ser realizada ya sea calentando el material adsorbido o evacuando el espacio sobre él. Existe un equilibrio entre las moléculas atrapadas y las que escapan.
Impartirle al material adsorbido la energía cinética para escapar o desorber es parte de la regeneración del adsorbente. Esta regeneración debe ser llevada a cabo antes de que todo el adsorbente sea incapaz de retener más, y debe ser realizada antes de que el adsorbente pueda ser utilizado de nuevo. La otra parte de la regeneración es el secado, el enfriamiento o la preparación del adsorbente de alguna otra manera para adsorber de nuevo al COV. |
| |
|
¿Qué es la Isotermia de Adsorción?
|
| |
| Cada adsorbente tiene una capacidad de adsorción a la que se le conoce como “isoterma de adsorción”. Históricamente, con el carbón, la isoterma se utilizaba para medir las libras de contaminante por libra de adsorbente que podía ser adsorbida a una temperatura dada. Sin embargo, la isoterma de adsorción también es una función de la concentración del contaminante, medida por la presión parcial del vapor y es también una función de la presión ambiental total alrededor del adsorbente. El número de moléculas que pueden ser almacenadas en el “pozo” depende de la presión, correspondiendo a mayor presión un menor espacio entre las moleculas adsorbidas. La isoterma de adsorción todavía se define como las libras de material que pueden ser adsorbidas por libra de adsorbente.
Los sistemas de regeneración térmica utilizan la isoterma de temperatura; los sistemas de regeneración al vacío utilizan la isoterma de presión total y parcial; y los sistemas de regeneración por oscilación de presión utilizan la isoterma de presión ambiental total. La “isoterma” es realmente una función de todas estas variables. Por lo tanto, la “isoterma” es realmente una función compleja que forma por lo menos una superficie tridimensional, en vez de ser una constante o una gráfica de dos dimensiones. La isoterma puede ser una función ya sea lineal o altamente no lineal, dependiendo del adsorbente, la presión, y el material que está siendo adsorbido.
La isoterma de adsorción también es una funcion de la cantidad de área de adsorción que pueden alcanzar las moléculas del COV. Los poros en la superficie permiten la entrada al área interior de cada uno de estos adsorbentes. Es en el interior donde existe la mayor área de adsorción. El carbón contiene poros que conducen a poros más pequeños, los que a su vez conducen a poros aún más pequeños. Esto aparentemente continúa ad infinitum en el carbón y la mayor parte de la superficie interna está en estos microporos. Las zeolitas tienen poros uniformes que son parte de su estructura cristalina. Los polímeros tienen poros dentro de un rango de tamaño, pero generalmente no tienen los pequeños microporos. Por tanto, la isoterma de adsorción es diferente para cada tipo de adsorbente y cada tipo de contaminante. |
| |
|
¿Cómo seleccionar un adsorbente?
|
| |
Existen muchos tipos de polímeros adsorbentes, muchos tipos de carbón adsorbentes y muchos tipos de zeolitas adsorbentes. Documentar todas estas variaciones haría de este documento todo un tomo y lo convertiría en un manual de operaciones en vez de un documento de conceptos. No tenemos la intención de describir adecuadamente todas las variaciones con tanto detalle. Solamente podemos tratar acerca de las propiedades generales y permitir que las selecciones específicas sean hechas por los diseñadores y sus clientes con la ayuda de los manuales correspondientes.
De interés primordial es el tamaño molecular más grande a ser adsorbido contra el tamaño de los poros del absorbente. Esto es particularemnte importante con las zeolitas, en las que los poros uniformes pueden ser de cualquier tamaño, desde 3 hasta 30 Ångstroms (0.3 a 3 nanómetros), dependiendo del tipo de zeolita. No debe esperarse que las zeolitas proporcionen alguna área de adsorción para moléculas mayores que sus poros, ni para moléculas por las cuales no tengan afinidad. El carbón y los polímeros deben también tener poros más grandes que la molécula más grande a ser adsorbida. Sin embargo, debido al rango más amplio de tamaño de los poros en el carbón y los polímeros, este criterio es menos estricto de lo que es para la zeolita. El área de adsorción a ser alcanzada por vía de los poros no debe ser tomada en cuenta si la molécula a ser adsorbida no puede ni alcanzarla ni ser desorbida de ésta.
Independientemente del método de regeneración, el área de adsorción no puede ser regenerada cuando la molécula adsorbida brinca desde un pozo en un lado del poro hasta un pozo del otro lado del poro. Esto puede ocurrir en los microporos del carbón y de algunos polímeros. Esto evitaría la desorción de las áreas donde los microporos se vuelven demasiado pequeños.
La afinidad del adsorbente por algunos tipos de sustancias puede ser mucho mayor que la afinidad por otras. Como resultado, cuando hay una afinidad fuerte por algunas de las moléculas, las moléculas que tienen menor afinidad se retendrán con una menor capacidad de adsorción o serán liberadas en favor de las moléculas por las cuales la afinidad sea mayor. El carbón, el cual no es ni completamente hidrofóbico ni hidrofílico, retiene alguna superficie de adsorción con afinidad tanto por las moléculas polares como por las no polares. Debido a ésto, la humedad tiene un efecto perceptible sobre el carbón. Un artículo de investigación hasta reporta que la desorción de COV del carbón ocurre mientras el vapor se condensa y el agua desplaza al COV.
Todas las zeolitas que existen en la naturaleza son hidrofílicas, teniendo una afinidad por las sustancias polares tales como el agua, pero las zeolitas sintéticas pueden ser hidrofílicas o hidrofóbicas. Los polímeros son generalmente hidrofóbicos, a menos que sean producidos específicamente con otra afinidad. Por ejemplo, los bloques de copolímeros anfofílicos pueden tener afinidades tanto hidrofílicas como hidrofóbicas. Por lo tanto, la afinidad debe ser considerada como parte de la selección de un adsorbente particular.
Algunos polímeros y las zeolitas hidrofóbicas son generalmente mucho menos sensibles a la humedad que los carbones y están también mucho menos sujetos a la posibilidad de incendio, desmoronamiento o pulverización. Por lo tanto, requieren ser reemplazados con mucha menor frecuencia. Los carbones son más baratos (al menos inicialmente). El costo por libra de carbón es de aproximadamente $2.00 dólares de EE.UU., lo cual es hasta 20 veces menos que el costo por libra ya sea de los polímeros o de las zeolitas. Sin embargo, la necesidad de reemplazar las zeolitas es muy rara y el reemplazo de los polímeros ocurre con una frecuencia solo ligeramente mayor. El carbón necesita ser reemplazado desde cada seis meses hasta cada cinco años o cuando suceda algún incendio del lecho. La frecuencia depende del tipo de carbón, la frecuencia de la regeneración y de la temperatura a la cual se opera.
La desorción térmica de algunos polímeros adsorbentes fue evaluada por la compañía General Electric Co. y se observó que éstos desorben más rapidamente que el carbón, que tienen una mayor capacidad de adsorción ya sea a una humedad alta o baja después del acondicionamiento y que desorben a temperaturas mas bajas. La temperatura máxima de desorción debe ser mayor que el punto de ebullicón del COV, pero no debe exceder el punto de fusión del polímero.
La temperatura máxima de desorción es menos limitante para el carbón, el cual puede elevarse a temperaturas mucho más altas (121 a 177 °C) sin fundirse. Cuando la temperatura excede este rango, el carbón frecuentemente cataliza reacciones de oxidación. Para las zeolitas se usa comúnmente la misma temperatura máxima, pero el límite real depende ya sea de la temperatura de pirólisis, de la temperatura de catalización de los COV adsorbidos o del rango de temperaturas en el cual la estructura cristalina de la zeolita es estable. Se considera que este rango de temperaturas metaestables es por lo general de hasta aproximadamente 534 °C (1000°F). |
| |
|
¿Existen otras consideraciones de diseño?
|
| |
|
¡SÍ! Estos otros factores se describen individualmente a continuación:
ZONA DE TRANSFERENCIA DE MASA
La zona de transferencia de masa (ZTM), véase la figura 3, existe en todos los adsorbentes. En la ZTM, la concentración de COV en el aire va desde el 100% de concentración de vapor a la entrada hasta la menor presión de vapor disponible en equilibrio con el adsorbente desorbido.
|
| La profundidad del lecho es la dimensión del adsorbente en la dirección del flujo del aire y la ZTM es por lo general mucho más corta que la profundidad del lecho. La ZTM se mueve a través del lecho a medida que el lecho alcanza su capacidad (se llena la isoterma de adsorción). Corriente arriba de la ZTM, el lecho ha alcanzado su capacidad, mientras que corriente abajo, el lecho permanece esencialmente sin adsorber. La saturación ocurre cuando la ZTM llega al final del lecho de adsorbente, corriente abajo. La saturación se observa como una elevación en la concentración de vapor de COV que abandona el lecho, lo cual puede ocurrir a diferentes tiempos para diferentes COV.
Los adsorbentes de todos los tipos comparten una característica con las columnas utilizadas en la cromatografía de gases, puesto que éstas también utilizan la adsorción. En cada sistema, el material adsorbido se desorberá espontáneamente y emigrará corriente abajo con el flujo de gas. Esto es causado por el gradiente de presión, el cual es intencionalmente muy bajo cuando los sistemas de adsorción son utilizados como tecnología de control de emisiones y más bien alto, en las columnas de adsorción en la cromatografía de gases. Esta migración de contaminantes es por lo general lo suficientemente lenta que puede ser despreciada durante el control de las emisiones. Sin embargo, esta propiedad define un tiempo máximo absoluto para la adsorción antes de regenerar el lecho. La saturación es realmente un proceso gradual, porque el equilibrio entre la presión de vapor y el adsorbente está variando continuamente. De este modo, la saturación puede ser definida como cualquier elevación notable en la concentración del efluente.
La ZTM también emigrará hacia la saturación independientemenete de la carga de COV. Un pico en la concentración de entrada de COV, junto con la migración de la ZTM, permitirá que el COV se distribuya y reducirá la concentración que será desorbida a la saturación. Un ejemplo de cómo pudiera un adsorbente utilizar la característica de migración de la ZTM, es en el flujo de aire de un extractor en una planta que maneja mercaptano. El gas natural es inoloro y se le añade mercaptano para crear una indicación por el olfato (olor) en caso de fuga. Si un derrame de mercaptano da lugar a emisiones en concentraciones mayores a una parte por billón, la gente podría olerlo y alarmarse porque pensarían que existe una fuga de gas. Por lo tanto, los extractores en los que se maneja el mercaptano están equipados con un adsorbente de tamaño adecuado. Este adsorbente captura cualquier vapor proveniente de derrames y, cuando la ZTM emigra hacia la saturación, el mercaptano es liberado a una concentración más baja en este caso. Esto es debido a que no fué una emisión continua de mercaptano; el adsorbente no agotó su capacidad y por lo tanto, la saturación ocurrió a una concentración menor que el valor del umbral de detección del olor. Para este propósito, la desorción o la regeneración no son necesarias a menos que los derrames sean demasiado frecuentes.
CAPACIDAD DE TRABAJO
Los “ciclos de acondicionamiento” son el número de ciclos (usualmente alrededor de cinco), que se requieren para alcanzar una cantidad estable de adsorción y de regeneración. El carbón, después de alcanzar los ciclos de acondicionamiento, es capaz de adsorber alrededor del 50% de la cantidad que fué adsorbida por el material virgen. Las zeolitas son capaces de adsorber alrededor del 90% de la cantidad adsorbida por el material virgen. Los polímeros pueden variar en el rango del 50% al 90%. Esta “isoterma acondicionada” también define la “capacidad de trabajo” del adsorbente. El hecho de que el carbón y algunos polímeros típicamente desorban sólo el 50% de lo que adsorbe el material virgen, se estima que sea debido a la recaptura continua de moléculas (ésto es, la reducción de la presión de vapor), en los microporos. El COV podría ser removido de estos microporos únicamente por medio de pirólisis, la cual destruiría el COV, además de que destruiría el polímero o alteraría las propiedades del carbón.
Las zeolitas tienen un tamaño de poros uniforme, por lo que no exhiben este fenómeno. Los polímeros tienen un rango más amplio de tamaños de poro y de cierta manera son similares a los carbones, pero se cree que algunos polímeros carecen de los pequeñísimos microporos. El carbón también muestra una distribución del COV en función del tiempo desde los macroporos hasta los microporos. Las zeolitas y los polímeros muestran esta distribución dependiente del tiempo en un grado mucho menos observable.
La “capacidad de trabajo” del adsorbente está determinada por la diferencia entre el nivel que tiene al regenerarse (desorbido), una vez acondicionado, y la isoterma de adsorción completa del adsorbente. Por tanto, el efecto del acondicionamiento debe ser considerado al determinar el tamaño del lecho de adsorbente. El efecto del acondicionamiento puede requerir hasta el doble de adsorbente en el lecho. Puesto que la regeneración debiera ocurrir solamente cada 8 o 16 horas de operación, la capacidad del (los) lecho(s) puede ser determinada por la concentración de COV, la velocidad del flujo de aire, el peso del adsorbente en el (los) lecho(s), el tipo de adsorbente y la “capacidad de trabajo” del adsorbente. De esta manera, la “capacidad de trabajo” puede tener un efecto significativo sobre el costo de la instalación, operación y mantenimiento de un sistema de adsorción.
PRESIÓN DE VAPOR
El carbón y los polímeros tienen una isoterma de adsorción lineal en relación a la presión de vapor, mientras que las zeolitas tienen una isoterma de adsorción bastante no-lineal en relación a la presión de vapor de las moléculas por las cuales tienen afinidad. Esta linearidad hace que el adsorbente, ya sea carbón o polímeros, sea el mejor cuando la presión de vapor (o la concentración) es más alta; pero la falta de linearidad hace que la zeolita sea el mejor adsorbente cuando la presión de vapor (o la concentración), es más baja. Esta propiedad permite el uso de adsorbentes de carbón o de polímeros en un lecho “de sacrificio” (o primero), seguido, en la dirección del flujo del aire, por una zeolita apropiada en un lecho “pulidor”, para producir la presión de vapor de COV más baja en la corriente de salida. Mientras más baja sea la presión parcial de COV a la salida, más alta será la eficiencia de control.
ADSORBENTES MÚLTIPLES
Existe también una ventaja en el uso de una mezcla de adsorbentes. Una mezcla de carbón y de zeolita removió mejor una mezcla de vapores de xileno y metanol que un adsorbente constituido de cualquiera de los dos. Hussey y Gupta de las Industrias Gurr reportaron ésto en la Reunión del American Institute of Chemical Engineers (Instituto Americano de Ingenieros Químicos), en la primavera de 1997. Ellos observaron que la trayectoria a través de la mezcla era más larga que la trayectoria a través de cualquiera de los adsorbentes cuando se utilizaron por sí sólos, y atribuyeron el aumento en la adsorción a la mayor longitud de la trayectoria. Sin embargo, tanto el metanol como el xileno fueron adsorbidos; y puesto que los autores declararon que los carbones adsorben bien al xileno mientras que una zeolita con un tamaño de poros de seis u ocho Ångstroms adsorbe bien al matanol, para producir este resultado, la profundidad debió haber sido la suma de las profundidades de los lechos individuales. En este artículo también se mencionó que a concentraciones altas, el carbón adsorbe mejor y puede ser utilizado como un lecho “de sacrificio” corriente arriba de un lecho “pulidor” de zeolita.
MODELOS DE ADSORCIÓN
Para determinar que tan bien funcionará el adsorbente seleccionado, el mismo debe ser sometido a una prueba con la mezcla de los contaminantes que se pretende adsorber y a las concentraciones que se espera tener. Esto debe realizarse ya sea si se usa únicamente un adsorbente o una combinación de adsorbentes. También debe llevarse a cabo para una mezcla de vapores de COV. Varios modelos de adsorción de multiespacios pueden predecir como adsorberá una combinación de COV, pero todos éstos están basados en las suposiciones que son válidas para los resultados del experimento en particular. Los ejemplos son de V. Gusev y J. O’Brien de la Unversidad de Yale; C. Jensen y N. Seaton de la Universidad de Cambridge; M. Heuchel de la Universidad de Leipzig. Debe comprobarse que los diferentes modelos de adsorción de multiespacios se aplican a su mezcla y concentración de COV y al adsorbente seleccionado.
INCENDIOS DEL LECHO
Toda adsorción es exotérmica; esto quiere decir que la adsorción desprende calor y causa una elevación de la temperatura. Esta propiedad ha sido utilizada para el almacenamiento de calor, pero no es deseable para la adsorción de COV. Se sabe que el carbón o los metales en el carbón, catalizan la oxidación de algunos contaminantes cuando el adsorbente está caliente, resultando en incendios del lecho que también consumen parte o todo el carbón. Esto es un riesgo cuando se adsorben ciertos hidrocarburos (tales como las cetonas o las terpentinas), a temperaturas ambiente que son cercanas a aquéllas que causan que se oxiden los COV. Tal incendio puede alterar el tamaño de los poros del resto del lecho u oxidarlo hasta hacerlo cenizas. Estos incendios han sido suprimidos mediante la humidificación del aire, dejando un poco de agua en el lecho después de una regeneración con vapor y por el enfriamiento intencional del carbón. Los polímeros son generalmente utilizados a temperaturas que no ocasionan incendios en el lecho, pero esto debe ser comprobado. Las zeolitas no so
|