Eliminación simultánea de hollín y óxidos de nitrógeno en efluentes de motores diesel
|
Introducción
|
Las partículas y los óxidos de nitrógeno son los principales contaminantes presentes en las emisiones de motores diesel.
Las partículas (TPM) están compuestas por sustancias carbonosas (“dry soot”), óxidos inorgánicos (principalmente sulfatos), y líquidos. Los líquidos son una combinación de combustible diesel no quemado y lubricante, llamados “Fracción orgánica soluble” (SOF), que se hallan adsorbidos en las partículas de hollín y también en forma de aerosoles.
Típicamente el SOF es un 55% del particulado total, conteniendo 20% de combustible y 35% de lubricante [1].
En la fase gas, además de óxidos de nitrógeno, las emisiones contienen monóxido de carbono e hidrocarburos, pero en menor proporción dada la mezcla oxidante utilizada en la combustión.
Es ampliamente conocido que los óxidos de nitrógeno contribuyen a la lluvia ácida y al smog fotoquímico, mientras que las partículas de hollín contienen compuestos químicos de probable actividad mutagénica.
Las leyes que regulan el contenido máximo de partículas y contaminantes gaseosos son cada vez más estrictas en todo el mundo, y dado que las emisiones diesel son más complejas en su composición que las de motores alimentados con nafta, su tratamiento requiere de la permanente aplicación de nuevas tecnologías. Los medios de transporte accionados por motores diesel son cada vez más populares debido a la eficiencia de combustible relativamente alta y la mayor durabilidad del motor si se compara con motores alimentados por nafta.
Los motores diesel operan usando mezclas oxidantes, con relaciones aire/combustible mayores a 20, lo que resulta en una combustión de relativamente baja temperatura que produce menores emisiones de NOx, CO e hidrocarburos.
Dada la economía de combustible, también la emisión de CO2 es menor que la producida por motores nafteros.
Debido a que el diseño del proceso de combustión resulta en altos niveles de emisión de partículas, en los últimos años se han realizado esfuerzos tendientes a mejorar el diseño del inyector de combustible .
Sin embargo, esto no ha sido suficiente para reducir la emisión de particulado a valores menores a los límites de las leyes actuales, por lo cual los tratamientos de post-combustión son necesarios [2].
Existen diversas tecnologías comerciales para el tratamiento de los efluentes de motores diesel.
Entre ellas, cabe mencionar la utilización de metales nobles depositados en monolitos cerámicos, los cuales son activos para la combustión de la fracción líquida (SOF), y para la oxidación del CO e hidrocaburos volátiles [3].
Sin embargo, con este método no es posible eliminar la fracción sólida del hollín (dry soot).
La tecnología EGR [4] es eficiente en disminuir la emisión de óxidos de nitrógeno y SOF, pero incrementa la emisión de sólidos.
La vía más factible para la eliminación de partículas es la utilización de filtros regenerables periódicamente [5].
La regeneración térmica por oxidación con aire requiere temperaturas mayores a 600°C lo cual origina severas tensiones en los materiales utilizados.
A fines de disminuir esta temperatura y realizar la regeneración contínua in situ es posible la utilización de catalizadores, los cuales pueden adicionarse al combustible en forma de moléculas organometálicas [6] o impregnarse en las paredes del filtro.
La primer alternativa tiene el inconveniente de la emisión de metales tóxicos, y con respecto a la segunda no se han desarrollado aún catalizadores suficientemente activos [7].
Recientemente, se ha anunciado la utilización comercial de filtros regenerados in situ mediante la oxidación del hollín con NO2 .
En esta tecnología, se utiliza un metal noble como catalizador para generar el NO2 mediante la oxidación catalítica del NO presente en los efluentes gaseosos del motor diesel .
La reacción entre el óxido nítrico y el hollín es no-catalizada y ocurre a 250°C.
Las limitaciones de esta tecnología se discutirán más adelante.
En una línea similar, se ha explorado a nivel de laboratorio [8-10] la reacción de eliminación simultánea del hollín y el NO (hollín + NO + O2 => nitrógeno + agua + dióxido de carbono).
Los resultados de estas investigaciones son altamente promisorios y son el objetivo principal de esta nota.
|
TECNOLOGIAS EN DESARROLLO
|
Las vías más desarrolladas para la reducción en la emisión de partículas son los catalizadores de oxidación y los filtros regenerables.
La utilización de catalizadores de oxidación, por ejemplo CeO2 soportado en monolitos [11] , permite una reducción importante de la fracción líquida presente en las partículas (SOF), lo cual constituye aproximadamente un 55% del TPM, pero estos sistemas no son eficientes para reducir la fracción seca (“dry soot”).
Los filtros cerámicos o metálicos permiten retener entre 70 y 95% de la emisión total de partículas.
Sin embargo, todavía existen considerables problemas de seguridad con respecto a la etapa de regeneración de los mismos, debido a las altas temperaturas que se pueden originar por la reacción de combustión [12].
La rápida acumulación del hollín en la superficie de los filtros, con el consecuente incremento de la caída de presión, necesita de la aplicación secuencial de un proceso de regeneración de manera de mantener la eficiencia del motor dentro de límites aceptables.
Los métodos de regeneración se pueden dividir en dos categorías :
• “Regeneración Activa” : mediante un quemador de combustible o una resistencia eléctrica.
• “Regeneración Pasiva” : aditivos en el combustible, catalizador monolítico antes del filtro, catalizador impregnado en las paredes del filtro.
Hasta el presente, debido a costos, simplicidad, requerimiento de espacios, y nivel de desarrollo de tecnologías, solo los filtros de partículas regenerados con aditivos en el combustible son considerados aplicables [12].
Luego de varios años de evaluación, los compuestos organómetálicos de cerio, cobre e hierro, son los candidatos más serios.
Esta tecnología tiene el inconveniente de la emisión a la atmósfera de los mencionados metales. Recientemente, Johnson Matthey ha comercializado un nuevo sistema aplicable a motores diesel que utilicen combustible con muy bajo contenido de azufre.
Este sistema, llamado CRT (Continuously Regenerating Trap), reduce emisiones de CO, hidrocarburos y partículas hasta un 90% y ha sido puesto a prueba en unidades de la Oxford Bus Company.
El mecanismo de funcionamiento del sistema CRT consiste en la oxidación del NO presente en los efluentes mediante un catalizador de platino soportado.
Luego el NO2 formado reacciona (sin catalizador) con las partículas de hollín retenidas en el filtro a temperaturas cercanas a 250°C, llevando a cabo el proceso de regeneración contínua.
Sin embargo, la reacción entre el hollín y el NO2 produce nuevamente NO, el cual es eliminado a la atmósfera. Por otra parte, el catalizador de este sistema es severamente envenenado con pequeñas cantidades de azufre, lo cual es una limitación para su uso.
No obstamte, dado el anuncio de que ARCO Products ofrece en Estados Unidos un combustible conteniendo como máximo 15 ppm de azufre, Johnson Mathey ha colocado su producto en el mercado de este país [13]. La reacción entre el NO2 y las partículas de hollín, fundamento de la operación del filtro CRT ha sido detalladamente estudiada a nivel de laboratorio por Lur’e y Mikhno [14].
Como conclusión, el sistema CRT tiene dos limitaciones: eliminación de NO a la atmósfera y alta sensibilidad al envenenamiento por azufre.
A continuación, se discutirá una nueva tecnología, la cual ha sido estudiada sólo a escala laboratorio, y que se basa en la regeneración contínua del filtro mediante la reacción catalítica hollín+NO+O2 , con el objetivo de eliminar ambos contaminantes en forma simultánea.
|
FUNDAMENTOS TEORICOS DE LA REACCION HOLLIN+NO+O2
|
Cuando están en contacto las partículas de hollín con una atmósfera gaseosa que contiene oxígeno y óxidos de nitrógeno, son posibles las siguientes reacciones: hollin+O2 , hollin+NO, hollin+NO+O2.
Shangguan et al [10] reportan los siguientes mecanismos para las mencionadas reacciones:
Mecanismo de la reacción C(hollín) + O2 Teniendo en cuenta un orden cinético de ½ obtenido para el oxígeno que fuera reportado en la bibliografía se plantea lo siguiente:
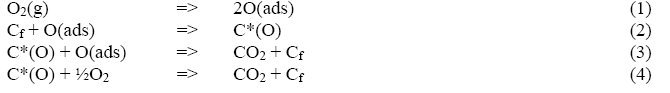
El oxígeno gaseoso es adsorbido disociativamente en la superficie (reacción 1).
Las especies atómicas resultantes atacan el sitio reactivo del carbón (Cf) para producir el intermediario C*(O) (reacción 2).
La reacción del intermediario con oxígeno adsorbido o bien con oxígeno gaseoso produce CO2.
Querini et al. [7] proponen a los carbonatos superficiales como intermediarios cuando se utilizan catalizadores básicos:
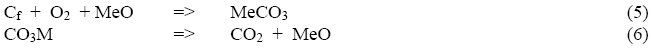
Donde MeO es un óxido metálico y MeCO3 es un carbonato superficial, detectable por FTIR.
Mecanismo de la reacción C(hollín) + NO
Mediante experimentos de reacción con temperatura programada, se halló que el orden de la reacción aumenta con la temperatura, y que existe un intermediario superficial que se forma entre el carbón y nitrógeno superficial.
Se propone el siguiente mecanismo consistente con los mencionados resultados:
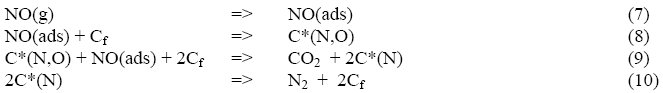
NO(ads) es el producto de la adsorción de NO, mientras que C*(N,O) y C*(N) son complejos superficiales de carbón que contienen los elementos mostrados entre paréntesis.
La alternativa a las reacciones (9) y (10) es :
![]()
Sin embargo, esta última reacción indicaría cantidades equivalentes de CO2 y N2 como productos, lo cual difiere de lo observado experimentalmente.
La reacción entre NO gaseoso y los intermediarios superficiales también es posible:
![]()
![]()
Mecanismo de la reacción hollín+NO+O2 Cuando se hallan presentes el oxígeno y el NO, a las etapas (1)- (13) deben adicionarse las reacciones:

Se ha observado experimentalmente [10] que la velocidad de la reacción (hollín+O2+NO) es mucho mayor que la de las reacciones (hollín+O2) y (hollín+NO) por separado.
Esto implica que la formación de NO2 mediante la reacción (14) juega un rol fundamental en el proceso.
|
ESTUDIOS DE LA REDUCCION SIMULTANEA DE HOLLIN Y NO A ESCALA DE LABORATORIO
|
Duriez y colaboradores [8], sintetizaron y caracterizaron una serie de óxidos mixtos con estructura perteneciente a la familia de las perovskitas con vistas a su utilización en la reducción de óxido nítrico con carbón.
Los tests catalíticos mostraron que, entre los sólidos estudiados, el óxido La2CuO4 perteneciente a la familia de estructura K2NiF4 es el más activo.
Desafortunadamente, en condiciones de reacción, este sólido se reduce parcialmente en La2O3 y CuO.
El origen de la alta actividad se halla en las propiedades intrínsecas de los iones de cobre, los cuales se hallan en el centro de un octaedro distorsionado con dos enlaces Cu-O lábiles.
Entonces se crean fácilmente vacancias de oxígeno donde se adsorbe preferencialmente el NO donde forma un intermediario con el carbón superficial el cual se descompone en nitrógeno y dióxido de carbono.
Estos estudios fueron realizados en ausencia de oxígeno.
Teraoka y colaboradores [9], utilizan en sus estudios una serie de perovskitas, algunas de las cuales contienen metales alcalinos (K, Cs, Li, Sr).
Los autores observan que las propiedades catalíticas de los diferentes sólidos se modifican notablemente según los cationes A y B utilizados para constituir la estructura perovskita (ABO3).
Con respecto a los metales alcalinos substituidos en estas estructuras, el potasio es el que otorga mayor actividad catalítica para la reducción de NO, pese a ser el sólido con menor área específica.
Dado que la eliminación simultánea de NO y soot ocurre en el llamado “triple punto de contacto” donde el catalizador sólido, las partículas de hollín y los reactivos de la fase gas (NOx y O2 ) se encuentran, la porosidad del catalizador es de poca importancia.
La relevancia del potasio como promotor de esta reacción se halla en el incremento de la superficie de contacto entre reactivos y, probablemente, en la activación de la superficie de las partículas de carbón.
Shangguan y colaboradores [10] realizan un cuidadoso estudio cinético de las reacciones hollín-O2, hollín-NO y hollín-NO-O2 sobre un catalizador CuFe2O4 con estructura de espinela.
A tal fin, utilizan la técnica de reacción con temperatura programada de mezclas hollín-catalizador.
Los autores hallan que el orden cinético con respecto al hollín es cero en todos los casos, mientras que con respecto al oxígeno el orden es 0,5.
Las expresiones cinéticas son las siguientes:
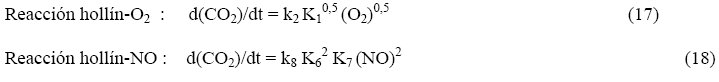
donde las k y K son las constantes específicas de velocidad de reacción y constantes de equilibrio (respectivamente) que corresponden a las etapas de los mecanismos mostrados más arriba.
En la reacción hollín-NO-O2 la velocidad de formación de CO2 depende de las concentraciones según (NO)0,6(O2)0,6 , y para la formación de N2 y N2O la función es (NO)1,0 (O2)0,4.
Las implicancias de la formación de NO2 es un aspecto que requiere más estudios para entender la cinética de la reacción.
|
DESARROLLO DE CATALIZADORES LIQUIDOS PARA LA OXIDACIÓN DE HOLLÍN
|
Es conocido que las deficiencias del contacto hollín-catalizador imponen severas restricciones en cuanto a la velocidad del proceso, sobre todo cuando éste se lleva a cabo en condiciones reales.
Si bien a nivel de laboratorio, trabajando con mortero o molino de bolas, es posible obtener una buena mezcla hollín-catalizador y por lo tanto un óptimo contacto en condiciones reales esto no es posible.
Una via que ha comenzado a ser explorada muy recientemente consiste en la utilización de sales, o mezcla de sales, que a la temperarura de operación del filtro se hallan en estado líquido, lo cual favorece notablemente el contacto y por lo tanto la velocidad de combustión de las partículas.
Jelles y colaboradores [15] realizan un estudio exploratorio con respecto a la eficiencia de sales fundidas como catalizadores para la oxidación de hollín.
Los autores midieron la actividad de dos eutécticos binarios con bajo punto de fusión en forma comparativa con la actividad de óxidos simples de alta actividad oxidante. Además, investigaron la influencia del NO sobre la velocidad de reacción.
Las sales fundidas Cs2MoO4-V2O5 y CsVO3-MoO3 resultaron más activas que CuO y MoO3, probablemente como resultado del incremento en la superficie de contacto debido al “mojado” de las partículas de hollín con las fases móviles del catalizador. La velocidad de combustión fue sensiblemente incrementada por la presencia de NO en la fase gas.
En este interesante trabajo, se propone el siguiente esquema para explicar el efecto promotor del óxido nítrico:
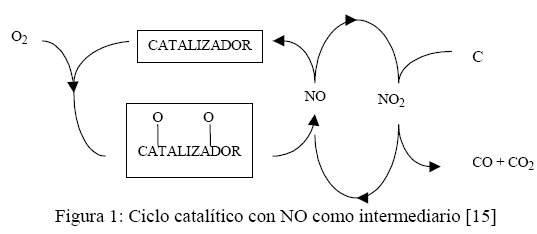
En este esquema no se incluye la conversión hacia N2 y N2O, la cual efectivamente ocurre en los catalizadores estudiados en las referencias antes citadas [8-10].
Una excelente revisión de esta temática, como asi novedosos resultados en este aspecto, pueden encontrarse en la tesis doctoral recientemente presentada por van Setten [16], y en publicaciones de su grupo [17-19].
Una de las sales más activas que ha sido reportada por dicho autor es el cloruro de cobre, el cual sin embargo no debe ser usado ya que al descomponerse y reaccionar con los gases residuales de la combustión promueve la formación de dioxinas.
En nuestros laboratorios, hemos estudiado la adición de potasio como promotor de un contacto eficiente hollín-catalizador, en particular en catalizadores basados en Co impregnado en CeO2 , La2O3 y MgO [20-22].
|
CONCLUSIONES
|
La eliminación simultánea de hollín y óxidos de nitrógeno mediante la reacción catalítica entre ambos es de interés para el desarrollo de nuevas tecnologías en el área de eliminación de contaminantes en efluentes de motores diesel.
Los catalizadores más activos reportados hasta el presente comienzan a quemar el hollín a relativamente bajas temperaturas (250-300°C), mientras que el óxido nítrico es convertido a N2 y N2O con una eficiencia de aproximadamente 50%.
Son necesarios aún más esfuerzos de investigación a nivel de laboratorio para mejorar la actividad y la selectividad en la reducción del NO, ya que el N2O es un contaminante que contribuye al efecto invernadero.
El deficiente contacto de las partículas de hollín con el catalizador bajo condiciones reales es una limitación que debe vencerse para obtener catalizadores suficientemente activos.
Agradecimientos:
el apoyo económico de la Universidad Nacional del Litoral y de la Agencia Nacional de Promoción Científica y Tecnológica es altamente agradecido.
|
BIBLIOGRAFIA
|
1- R. M. Heck, R. J. Farrauto, “Catalytic Air Pollution Control”, Van Nostrand Reinhold 1995.
2- R.J. Farrauto, R.N.Heck, B.Speronello, Chemical and Engineering News 70, 36 (1992)
3- N.Hawker, Platinum Metals Review 39, 1 (1995) 2
4- J.C.Summers, S. Van Houtte, D.Psaras, Applied Catalysis B:Environmental 10 (1996) 139.
5- J.Widdershoven, F.Pischinger,G.Lepperhof, SAE paper 860013.
6- K.N.Pattas, A.M.Stamatelos, SAE paper 910137.
7- C.A.Querini, M.A.Ulla, F.Requejo, J.Soria, U.Sedrán, E.E.Miró, Applied Catalysis B:Environmental 15 (1998) 5.
8- V.Duriez, L.Monceaux, P.Courtine, Catalysis and Automotive Pollution Control III, Studies in Surface Science and Catalysis 96 (1995) 137.
9– Y.Teraoka, K.Nakano, S.Kagawa, W.F.Shangguan, Applied Catalysis B:Environmental 5 (1995) L181.
10- W.F.Shangguan, Y.Teraoka, S.Kagawa, Applied Catalysis B:Environmental 12 (1997) 237.
11- R.J.Farrauto, K.E.Voss, Applied Catalysis B:Environmental 10 (1996) 29.
12-P.Zelenka, W.Cartellieri, P.Herzog, Applied Catalysis B:Environmental 10 (1996) 3.
13- http://www.dieselnet.com/news/9912jm2.html, 2001
14- B.A.Lur’e, A.V.Mikhno, Kinetics and Catalysis 38, 4 (1997) 535.
15- B.A.A.L. van Setten, “Development of a liquid catalyst for Diesel soot oxidation. From podwer to prototipe”, tesis doctoral presentada en Technische Universiteit Delft.
16- S.Jelles, B.A.A.L. van Setten, M.Makkee, J.A.Moulijn, Catalysis and Automotive Pollution Control IV, Studies in Surface Science and Catalysis 116 (1998) 667.
17- S.J.Jelles, B.A.A.L. van Setten, M.Makkee, J.A.Moujlin, Appl.Catal.B:Environmental 21(1999)35.
18- B.A.A.L. van Setten, J.Bremmer, S.J.Jelles, M.Makkee, J.A.Moujlin, Catal.Today 53(1999)613.
19- B.A.A.L. van Setten, J.M.Schouten, M.Makkee, J.A.Moulijn, Appl.Catal.B:Environmental 28(2000)253.
20- C.A.Querini, L.M.Cornaglia, M:A. Ulla, E.E. Miró, Appl. Catal. B: Env. 20(1999)165-177
21- E.Miró, F.Ravelli, M.A.Ulla, L.M.Cornaglia, C.A.Querini, Stud. Surf. Sci. Catal. 130(2000)731
22- E.Miró, F.Ravelli, M.A.Ulla, L.M.Cornaglia, C.A.Querini, Catal. Today 53(1999)631.
Eduardo E. Miró y Carlos A. Querini
Instituto de Investigaciones en Catálisis y Petroquímica-INCAPE(FIQ,UNL,CONICET)
Santiago del Estero 2829, (3000) Santa Fe, Argentina.