Degradación de Plaguicidas
Sixto Malato Rodríguez, Julián Blanco Gálvez, Claudio A. Estrada Gasca y Erick R. Bandala
1. PROBLEMÁTICA AMBIENTAL
El incremento en la producción y uso de compuestos químicos en los últimos cien años ha dado origen a una preocupación creciente sobre el efecto que dichos compuestos pueden tener sobre los ecosistemas terrestre y acuático (Figura 1). Debido a sus características químicas, los plaguicidas son contaminantes persistentes que resisten en grado variable la degradación fotoquímica, química y bioquímica, por lo que su vida media en el ambiente puede ser elevada [1-3]. La aplicación de plaguicidas sintéticos ha sido una práctica rutinaria en la agricultura en los últimos cincuenta años. El uso indiscriminado que en el pasado se ha dado a estos compuestos, ha producido que en la actualidad se detecten residuos de estos en el ambiente y se asocien con riesgo potencial a la salud pública [4].
 |
Actualmente los residuos de estos plaguicidas han sido identificados en todo los compartimientos ambientales (aire, agua y suelo), en todas las regiones geográficas incluyendo aquellas muy remotas al sitio original de su liberación ambiental, como océanos, desiertos y zonas polares. Igualmente se ha demostrado su presencia en organismos de todos los niveles tróficos, desde el plancton hasta las ballenas y los animales del ártico. Estos compuestos se bioacumulan en numerosas especies y se han biomagnificado a través de todas las redes tróficas del mundo. Los seres humanos no están exentos de esta contaminación y los plaguicidas se han podido identificar en diversos tejidos y secreciones humanos, inclusive de los habitantes de regiones muy aisladas [3].
Existe una gran cantidad de informes en los cuales se alerta sobre la amplia distribución de plaguicidas en el mundo [5-7]. En los países en desarrollo hay enormes cantidades de plaguicidas tóxicos y/o obsoletos, que son un peligro mortal para la salud humana y el medio ambiente. Se calcula globalmente que hay cientos de miles de toneladas de plaguicidas obsoletos, y que más de 100.000 toneladas de ese total está en los países en desarrollo [8]. Los plaguicidas que deterioran el paisaje urbano y rural de los países en desarrollo son: aldrin, DDT, dieldrin, endrin, fenitrotion, HCH, lindano, malatión y paratión entre muchos otros. La mayoría de las personas conocen el peligro del DDT, sin embargo se asegura que el dieldrin es cinco veces más tóxico que el DDT al ingerirse, y 40 veces más tóxico si se absorbe por la piel. El endrin es 15 veces más tóxico que el DDT para los mamíferos, 30 veces más tóxico para los peces y hasta 300 veces más tóxico para algunas aves [3].
Por lo general, la aplicación final de los plaguicidas la hacen personas poco informadas, más pobres y menos capaces de protegerse. A menudo los bidones se guardan a la intemperie, junto a almacenes de alimentos o mercados y donde los niños tienen fácil acceso a ellos. Estas reservas olvidadas son un grave peligro. Podrían producir una tragedia en las zonas rurales y en las grandes urbes. Como resultado, no debe sorprender que la agricultura sea una ocupación peligrosa. En Estados Unidos, una de las pocas naciones de América donde se tiene registro de este tipo de problemas, la tasa de mortalidad entre los trabajadores agrícolas en toda la nación está estimada en 20,9 por cada 100.000, debido a la exposición a los plaguicidas, que es mayor que en cualquier otro segmento de la población [9].
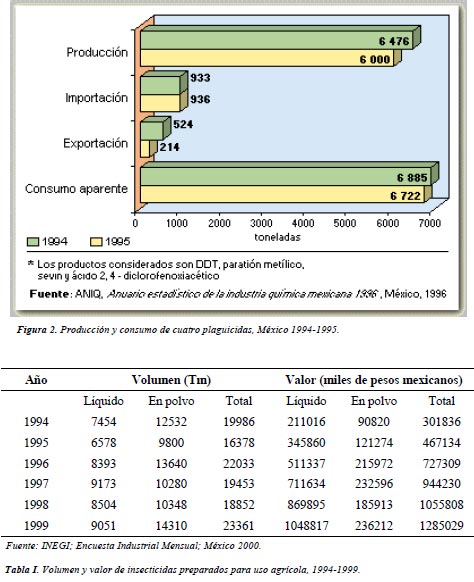
Los informes de las Naciones Unidas estiman que de todos los plaguicidas usados en la agricultura, menos del 1% alcanza los cultivos. El resto termina contaminando la tierra, el aire y, principalmente, el agua. Como estos contaminantes son habitualmente no biodegradables y sólo una pequeña cantidad de los residuos son tratados actualmente (por la carencia de tecnologías de tratamiento disponibles in-situ), existe un gran problema de acumulación de consecuencias no predecibles en un futuro de cercano. No obstante todas las características nocivas de estos compuestos, la venta de plaguicidas en todo el mundo aumenta sustancialmente todos los años, sobre todo en los países en desarrollo. En 1996, las ventas mundiales de esta industria fueron de 33.000 millones de dólares de las cuales mas del 70 % por ciento se consume en países en vías de desarrollo. El uso de plaguicidas en Centroamérica, es una práctica creciente. En México por ejemplo, aunque la producción de plaguicidas ha estado disminuyendo, en 1996 se generaron alrededor de 6.000 toneladas de tan sólo cuatro plaguicidas, y su consumo aparente durante ese año fue superior a las 6.700 toneladas (Figura 2) [10]. La venta y el consumo de DDT, plaguicida organoclorado de uso restringido en muchos países desarrollados, se ha mantenido con fluctuaciones alrededor de las 1000 toneladas anuales desde la década de los 80 y aún es empleado profusamente en la prevención del paludismo [11]. En total, el volumen de insecticidas preparados solamente para uso agrícola ha variado entre 16400 toneladas como mínimo durante 1995 hasta 23300 toneladas como máximo en 1999 (Tabla I) [12].
 |
Otro ejemplo importante de problemas relacionados con los plaguicidas se encuentra en las actividades de la agricultura intensiva (invernaderos) propias de países industrializados. Este sector está creciendo exponencialmente durante los últimos años en el área mediterránea de la Unión Europea donde existen más de 150000 hectáreas de invernaderos en la actualidad. Esta actividad necesita aproximadamente 200 veces más plaguicidas que la agricultura tradicional. Así, hay una creciente concienciación pública del daño ambiental relacionado con la agricultura intensiva. Los problemas medioambientales asociados son una de las amenazas más críticas para el futuro de este sector, tan importante económicamente.
2. TECNOLOGÍAS DISPONIBLES Y LIMITACIONES
Es urgente el desarrollo de tecnologías simples, de bajo costo y eficientes para la eliminación in situ de estos contaminantes en el ambiente. Actualmente estas tecnologías no existen y el tratamiento de, por ejemplo, efluentes para la eliminación de estos contaminantes es extraordinariamente caro. Como ejemplo, la FAO ha calculado que eliminar una tonelada de plaguicidas cuesta entre 3500 y 4000 dólares [8]. En la actualidad se han propuesto alternativas para reducir el consumo de plaguicidas como la modificación de las prácticas agrícolas, el uso de cultivos resistentes o el control biológico de las plantas. Sin embargo, en la mayoría de los países en desarrollo estos medios de combate de plagas son utilizados muy poco tal vez debido a la cultura o las políticas agrícolas de estos países [13], y muy a menudo por cuestiones de falta de recursos económicos.
Existen diversas tecnologías para la destrucción de plaguicidas, que van desde tratamientos físicos como la adsorción y filtros percoladores, hasta tratamientos biológicos y procesos avanzados de oxidación (ver Capítulo 1). Las operaciones de tratamiento terciario, actualmente implantadas en las depuradoras, como ósmosis inversa o adsorción con carbón activado (procesos que obtienen una fracción diluida y otra muy concentrada en el contaminante, aunque no lo degradan), muy a menudo, parecen no ser suficientemente eficaces para conseguir aguas con un mínimo contenido en los contaminantes más persistentes (plaguicidas, fenoles, disolventes, etc.). Por ello, resultan necesarias otras etapas de tratamiento que logren este objetivo. Los intervalos de concentración (de manera general) en los que son aplicados cada una de estas tecnologías fueron mostrados en la Figura 6 del Capítulo 3.
Dentro del marco de referencia dado en el Capítulo 3, los tratamientos de oxidación avanzada posiblemente constituyan en un futuro próximo uno de los recursos tecnológicos más utilizados en el tratamiento de aguas contaminadas con productos orgánicos procedentes de efluentes industriales (industrias químicas, agroquímicas, textiles, de pinturas, etc.), que no son tratables mediante técnicas convencionales debido a su elevada estabilidad química y/o baja biodegrabilidad.
Centrando nuestra atención en los plaguicidas, algunos de ellos, son razonablemente degradables usando tecnologías que no son fotocatalíticas. Por ejemplo, los piretroides como el permetrin se degradan hasta en un 65% mediante procesos de ozonólisis [14] Los plaguicidas triazínicos como atrazina, simazina y promazina han sido degradados utilizando ozono en ausencia de luz y mediante la combinación O3/H2O2 aumentando, por este último proceso, la velocidad de la reacción [15]. Algunos plaguicidas carbámicos han sido transformados en derivados de menor toxicidad en presencia de peróxido de hidrógeno y complejos de Fe(III) [16], mediante la aplicación de radiación UV en presencia de oxígeno [17] y peróxido de hidrógeno [18]. Muchos otros plaguicidas de diversas estructuras han sido degradados mediante procesos de oxidación avanzada como irradiación directa con luz solar [19-20] y ozono/Fe (III) [21].
A pesar de sus ventajas, esas tecnologías de tratamiento también presentan algunos inconvenientes que es preciso puntualizar. El empleo de lámparas fluorescentes de luz ultravioleta para llevar a cabo la irradiación de los efluentes a tratar puede aumentar los costos de operación hasta más de tres veces por arriba del costo de operación del proceso utilizando radiación solar [22]. La aplicación de tecnologías que utilizan solo agentes oxidantes como el ozono o el peróxido de hidrógeno no es lo suficientemente eficiente para la eliminación de los residuos de plaguicidas [23]. Puesto que el potencial de oxidación de éstos es menor que el de su combinación con radiación UV, a menudo no son capaces de llevar a cabo la mineralización completa de los contaminantes, y generan residuos que podrían presentar complicaciones ambientales adicionales como alta toxicidad, persistencia, bioacumulación o biomagnificación.
Otra de las alternativas de tratamiento que ha sido analizada para la degradación de estos contaminantes es la aplicación de la biotecnología [24]. La aplicación de cepas puras y consorcios microbianos a la degradación de plaguicidas ha sido llevada a cabo para una amplia variedad de sustratos. Plaguicidas clorados como toxafeno, aldrin, dieldrín, heptacloro y epóxido de heptacloro, 2,4-D y DDT, entre otros han sido degradados aceptablemente utilizando procesos biológicos. En algunos casos, los porcentajes de degradación obtenidos aplicando este tipo de procesos biológicos son de hasta 97% o mineralización de hasta 79% [4, 13 ,25-26]. A pesar de los resultados alentadores, esta tecnología presenta inconvenientes como largos tiempos de procesos (alrededor de 200 horas en los ejemplos anteriores) y la necesidad de etapas prolongadas de adaptación del sistema al ambiente tóxico provocado por el contaminante. El primer factor es un inconveniente relativamente menor, puesto que dichos tiempos son comparables a los tiempos de aplicación de procesos biológicos a la degradación de otros contaminantes menos recalcitrantes que los plaguicidas. El segundo factor, sin embargo, es un serio inconveniente, puesto que involucra largos periodos de adaptación del microorganismo a las condiciones adversas que genera la presencia del contaminante en el efluente. Además, restringe el sistema de tratamiento a los contaminantes para los cuales se ha llevado a cabo la adaptación de la cepa
3. DEGRADACIÓN DE PLAGUICIDAS MEDIANTE FOTOCATÁLISIS
La descontaminación fotocatalítica solar es en la actualidad una de las más exitosas aplicaciones de la fotoquímica solar. Corrobora este hecho la variedad de instalaciones y proyectos que están actualmente en operación [27-30].
El grupo de los plaguicidas, comprende una gran gama de sustancias químicas. Como ya se dijo (ver Capítulo 3), algunos de ellos son solubles en agua, otros se usan en suspensión, disueltos en compuestos orgánicos, en polvo, etc. No obstante, la mayoría de ellos se disuelven, suspenden o emulsifican en agua antes de aplicarse y la cantidad de agua residual que producen varía mucho dependiendo de la naturaleza y el manipulado que se hace en los diferentes procesos, como el enjuagado y limpieza de los tanques de los equipos de pulverización, vertido de los sobrantes de las aplicaciones, reciclado de los envases, etc. La destrucción de plaguicidas residuales se han mostrado como uno de los mejores campos de aplicación de la tecnología de descontaminación solar. Esta técnica puede calificarse de “omnívora”; ya que puede tratar disoluciones de baja concentración de compuestos puros o suspensiones de formulaciones comerciales multicomponentes. Además de la gran cantidad de residuos de plaguicidas generados en la agricultura, existe también una enorme cantidad de residuos provenientes de las factorías que producen los ingredientes activos y, especialmente de las factorías donde los componentes activos y otros compuestos del formulado son almacenados, mezclados, y envasados. Se ha ensayado ya la degradación mediante fotocatálisis con TiO2 de más de un centenar de plaguicidas. Entre ellos, los más ampliamente estudiados son los organoclorados, organofosforados, carbamatos, tiocarbamatos, triazinas, etc. La Tabla II reúne la mayoría de la información disponible en la literatura científica sobre la tecnología de fotocatálisis con TiO2 aplicada a la descontaminación de aguas que contienen estos compuestos.
 |
A continuación se presentan algunos ejemplos de degradación de plaguicidas (metamidofos, y pirimetanil) con radiación solar y en la planta piloto en la Plataforma Solar de Almería (PSA). La configuración actual del campo de CPCs (ver Capítulo 3) de la PSA tiene 6 módulos (superficie total de colectores de Ar = 8,9 m2, volumen de fotorreactor de 108L, volumen total de planta de Vt = 247 L) montados en una plataforma fija inclinada 37º (latitud local). Esta planta ha estado operando desde 1994 como se ha descrito en detalle en otros trabajos anteriores [130-131]. Los ejemplos a discutir incluyen un caso de comparación de la descomposición de un producto puro con un producto comercial y un estudio del producto comercial únicamente por la imposibilidad de disponer de compuesto puro en suficientes cantidades para realizar ensayos en planta piloto. . Se presentan dos enfoques totalmente distintos de la experimentación en este campo. En el caso del metamidofos se muestra cómo realizar experimentos cuyo objetivo sea obtener los parámetros necesarios para diseñar el proceso de mineralización (y por tanto descontaminación). En el otro caso (pirimetanil), se busca determinar, con mayor exactitud posible, el mecanismo de reacción mediante la aplicación de técnicas analíticas complejas, para identificar la posible acumulación de diversos productos de degradación parcial. Además, se estudia la factibilidad de utilizar peroxodisulfato como oxidante, para acelerar la reacción fotocatalítica (ver Capítulo 3). A continuación se describe el procedimiento empleado en todos los casos para evaluar la cantidad de radiación incidente.
Las constantes cinéticas de los procesos fotocatalíticos pueden ser obtenidas mediante la representación de la concentración de sustrato en función de tres variables diferentes: tiempo, radiación incidente dentro del reactor y flujo fotónico absorbido por el catalizador.
Dependiendo del procedimiento, la complejidad de estas constantes varía tanto como su aplicabilidad. Cuando se usa el flujo fotónico absorbido por el catalizador como variable independiente, la extrapolación de los resultados es mejor. Sin embargo, este procedimiento requiere conocer algunos parámetros como el número de fotones incidentes que pasan a través del reactor sin interacción con el catalizador, la dirección de la luz dispersada, la distribución de tamaño de las partículas suspendidas en el líquido, etc (ver Capítulo 9). Tales requerimientos tornan impracticable el procedimiento para el reactor usado para estos experimentos. El uso del tiempo experimental como unidad de cálculo podría originar errores en la interpretación de los resultados, ya que el reactor tiene elementos iluminados y no iluminados. Los reactores experimentales tan grandes como el utilizado en este trabajo, requieren mucha instrumentación y el reactor debe ser también lo más versátil posible, lo cual incrementa sustancialmente el volumen no iluminado. Usando el tiempo de residencia, que es el tiempo que el agua está expuesta a la radiación, las conclusiones también pueden llegar a ser erróneas, ya que, al usar el tiempo como la variable independiente, las variaciones en la radiación incidente en el reactor durante un experimento no son tomadas en cuenta.
La intensidad de la radiación solar ultravioleta (UV) es un parámetro esencial para la evaluación correcta de los datos obtenidos durante los experimentos fotocatalíticos en una planta piloto de descontaminación solar de agua. Consecuentemente, la cantidad de energía recogida por los colectores (por unidad de volumen, kJ L-1) desde el comienzo del experimento hasta que cada muestra es tomada, QUVn , puede expresarse mediante la ecuación (1), donde UVG,n es la intensidad media de la radiación UV en el intervalo de tiempo Δtn, Ar es el área de los colectores solares del reactor, Vt es el volumen total del reactor y Δtn = tn – tn – 1 es el intervalo entre los tiempos en que se toman las muestras n-1 y n.
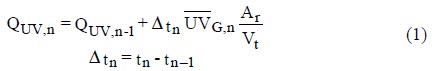 |
Para evaluar UV G,n , se ha utilizado un sensor de medida de la radiación global UV (KIPP&ZONEN, modelo CUV3) montado en una plataforma fija inclinada 37º (el mismo ángulo que los CPCs). Estos radiómetros proporcionan datos en términos de radiación incidente, WUV m-2, los cuales dan una idea de la energía que reciben las superficies que están en la misma posición que él con respecto al sol.
3.1. Tamaron
Una de las formulaciones comerciales elegidas es Tamaron (metamidofos, órganofosforado). Tamaron 50 contiene metamidofos 50% p/v y otros orgánicos no especificados por el fabricante. Una disolución acuosa de 0.33 mL/L de Tamaron tiene un COT de 100 mg/L (sólo 28 mg/L son de metamidofos). Se realizan dos tipos de experimentos siempre con una concentración de TiO2 de 200 mg L-1 y un COT0= 100 mg L-1: Degradación fotocatalítica sólo con TiO2, y con la adición de 10 mM de S2O8 2-. La reacción de mineralización para el metamidofos es:
|
|
La descomposición del metamidofos libera una cantidad equivalente de fosfatos (1 mol de fosfato por mol de metamidofos). Por esta razón, se mide la concentración de fosfato para evaluar el grado de mineralización del plaguicida. No es conveniente usar las mediciones de la concentración de sulfato porque la descomposición del peroxodisulfato aporta cantidades adicionales de sulfatos bastante elevadas.
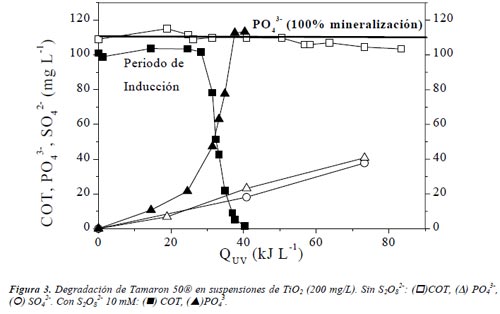 |
No se consigue una significativa mineralización con el uso de catalizador (TiO2) sin S2O8 2-: sólo el 10 % del COT0 (aproximadamente un 36 % del plaguicida) es degradado con 75 kJ L-1 de energía acumulada (650 min. de irradiación). El ensayo con peroxodisulfato supone una mejora correspondiente a un factor de 18 veces en la velocidad de mineralización con respecto al ensayo sin S2O8 2-.
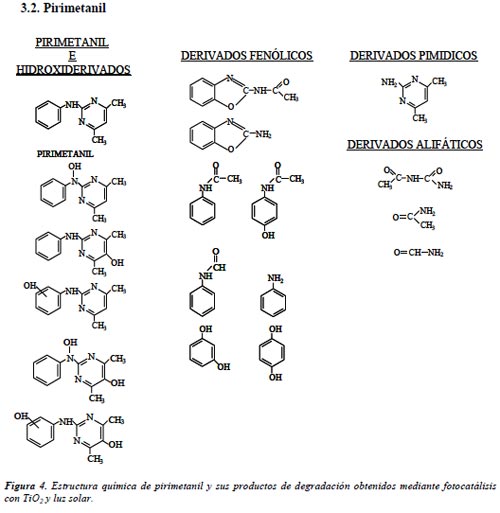 |
En el caso del pirimetanil se estudia la degradación fotocatalítica con TiO2 de disoluciones acuosas de pirimetanil técnico (98,2 % de pureza) y de la formulación comercial (Scala, 40 % pirimetanil). Se ha llevado a cabo un estudio cualitativo y cuantitativo de los productos de degradación generados durante el proceso mediante la utilización de cromatografía de gases acoplada a espectrometría de masas (GC-MS) y cromatografía de líquidos acoplada también a espectrometría de masas (LC-MS). Han sido detectados como intermedios de degradación 22 compuestos (de los cuales se han identificado 17). Para evaluar la eficacia del proceso de extracción de esos productos de degradación en disolución acuosa, especialmente para los productos más polares, se ha realizado un estudio de recuperación con pirimetanil y siete de los productos de degradación que están disponibles en el mercado como productos puros. Han sido comparadas la extracción líquido-líquido (LLE) y la extracción en fase sólida (SPE), con diferentes materiales. Se han propuesto dos caminos principales en el proceso de degradación: (i) ataque de los radicales hidroxilo al anillo bencénico y pirimidínico; (ii) hidrólisis fotoinducida de la molécula por los enlaces del grupo amino.
4. CASO PRÁCTICO. RECICLADO DE ENVASES DE PLAGUICIDAS [132-133].
Este caso está enfocado específicamente en los problemas derivados de las actividades de la agricultura intensiva (invernaderos). Los problemas medioambientales asociados son una de las amenazas más críticas para el futuro de este sector, tan importante económicamente. Una de estas consecuencias medioambientales se deriva de la eliminación de las botellas de plástico de los plaguicidas que todavía contienen pequeñas cantidades residuales de éstos. Normalmente, la mayoría de dichas botellas son mezcladas con los residuos convencionales de la agricultura o simplemente vertidas sin control. El reciclado de estos envases de plástico para otros usos ofrece una posible solución para este problema. Tras la recogida selectiva, los plásticos deben ser lavados antes de procesarlos para su nuevo uso, dando lugar a agua contaminada con una mezcla de diferentes plaguicidas que debe ser tratada. La eficiencia del proceso energía-solar/TiO2 ya ha sido probada en experimentos a escala de planta piloto Aunque este ejemplo se concentra especialmente en el reciclado de envases de plaguicidas usados en el área de El Ejido (Almería, España), donde la agricultura intensiva (400 km2 de invernaderos) consume aproximadamente 1,5 millones de envases de plástico de plaguicidas al año, pretende ser sólo un ejemplo de aplicación para validar la tecnología propuesta. Los resultados obtenidos podrían ser aplicados a otros casos de contaminación de aguas por plaguicidas y podría también aplicarse a una gran cantidad de sustancias altamente contaminantes similares distribuidas actualmente en contenedores.
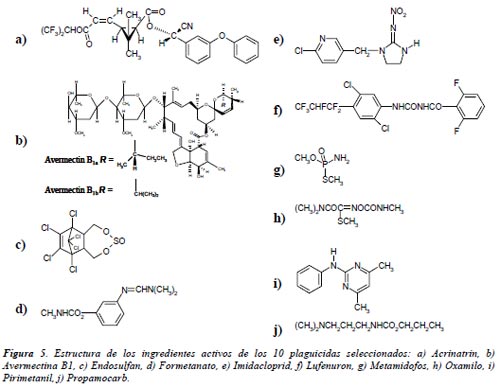 |
Las aguas de lavado simuladas fueron preparadas por combinación de diez formulaciones diferentes (Figura 5): Rhône-Poulenc Rufast® (Acrinatrin, C26H21F6O5, piretroide, 15% p/v), Merck Vertimec® (Avermectina B1, C48H72O14, sin familia, 1,8% p/v), AgrEvo Thiodan® (Endosulfan-α-β, C9H6Cl6O3S, organoclorado, 35% p/v), AgrEvo Dicarzol® (Formetanato, C11H16ClN3O2, carbamato, 50% p/v), Bayer Confidor® (Imidacloprid, C9H10ClN5O2, sin familia, 20% p/v), Ciba-Geigy Match® (Lufenuron, C17H8Cl2F8N2O3, benzoilurea, 5% p/v), Bayer Tamaron 50® (Metamidofos, C2H8NO2PS, organofosforado, 50% p/v), Dupont Vydate® (Oxamilo, C7H13N3O3S, oxima de carbamato, 24% p/v), AgrEvo Scala® (Pirimetanil, C12H13N3, anilinopiridina, 40% p/v) y AgrEvo Previcur® (Propamocarb, C9H20N2O2, carbamato, 72,2% p/v). Estos productos se usaron sin purificación, es decir que todas las impurezas y aditivos contribuyen al contenido de carbono orgánico total (COT). El contenido de COT de cada formulación fue determinado en experimentos preliminares. Los 10 productos comerciales elegidos han sido seleccionados porque son ampliamente usados en el área de El Ejido, pertenecen a las familias de plaguicidas más usuales y/o tienen una estructura química muy diferente. En todos los experimentos fueron añadidas iguales cantidades de COT (por ejemplo, 10 mg/L) de cada plaguicida para lograr la concentración inicial de COT deseada (por ejemplo, 100 mg/L).
Algunos de los pesticidas normalmente se adhieren a las paredes del reactor por su carácter hidrofóbico, y como consecuencia la medida de TOC inicial era algo baja al principio del tratamiento para alcanzar un máximo (COTmax) a los pocos minutos de iluminación. Por lo tanto en este trabajo se usó el COTmax en lugar del COT inicial para los cálculos.
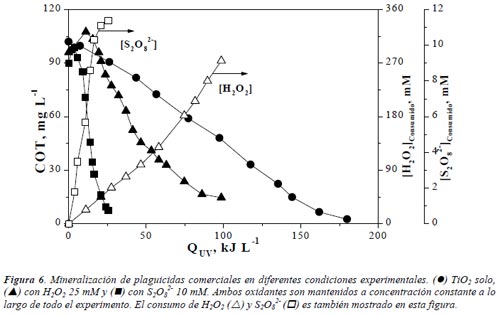 |
En la Figura 6 se muestra el efecto de la adición de captadores de electrones (hidrógeno peróxido y peroxodisulfato). El peroxodisulfato ha sido elegido como adecuado debido a la mejora obtenida en la velocidad de la reacción de mineralización, el consumo relativamente bajo de este reactivo y la no influencia de la relación molar S2O8 2-/contaminante en la velocidad de reacción (en el caso del hidrógeno peróxido siempre hay una relación óptima que suele ser difícil de mantener a lo largo de la degradación). La información obtenida permite optimizar el uso del peroxodisulfato para obtener resultados fiables, y decidir si usar o no este reactivo para incrementar la velocidad de mineralización. Después de un periodo de inducción, el carbono orgánico total en transformado es CO2. Los valores de COT descienden rápidamente hacia 0 en presencia de peroxodisulfato 10mM, sugiriendo que la adición acelera fuertemente la degradación de intermedios. Se logra así una reducción muy importante de la energía necesaria para la mineralización total dada por la ecuación (1) (al menos 6 veces para COT inicial alrededor de 100 mg/L). Esta reducción puede traducirse en una reducción equivalente de la superficie de colectores necesaria para degradar los orgánicos en el agua de proceso. La concentración inicial máxima ha sido establecida como 100 mg/L porque a esta concentración los plaguicidas comerciales producen una espuma apreciable en el agua y esto produce problemas de operación en la planta piloto. Además, el objetivo de esta investigación es el tratamiento de aguas residuales procedentes de una planta de reciclado de envases de plaguicidas y estos problemas se producirán también en esta planta. Por lo tanto, 100 mg/L ha sido considerada como la concentración máxima a tratar.
Como la reacción no sigue un modelo simple que conduzca a expresiones cinéticas sencillas (por ejemplo, de orden uno o cero) no se puede calcular una constante de velocidad de reacción. El COT es un parámetro global, que refleja la formación y descomposición simultánea de muchos, a veces varios cientos de productos. Para obtener una herramienta práctica para la comparación de varios experimentos, han sido elegidos dos parámetros diferentes: En primer lugar la energía acumulada necesaria para alcanzar un grado de mineralización determinado (QUV, X%COT se define como la energía acumulada incidente sobre el reactor por unidad de volumen necesaria para mineralizar X% del COT máximo). Por otro lado, es conveniente el uso de la pendiente máxima de la curva de degradación, que es formalmente la pendiente de la tangente en el punto de inflexión (rQ,0). Esta magnitud tiene las dimensiones de una constante de velocidad de orden cero (mg/kJ en lugar de mg/min, ya que se usa QUV y no tiempo como variable independiente), y por lo tanto es de manejo simple.
Esta pendiente puede ser considerada aproximadamente como la velocidad inicial de la reacción de mineralización.
Como se ha comentado, el área de El Ejido (Almería) consume aproximadamente 1.5 millones de botellas de plástico de plaguicidas por año. Como el tratamiento fotocatalítico propuesto en este trabajo está enfocado al tratamiento de la cantidad de producto que queda e