Contaminación del aire urbano: efectos de la radiación solar
RESUMEN
En este trabajo se presenta un estudio de los efectos fotolíticos en cámara de ambiente controlado y la formación y reacción del ozono en presencia de diferentes contaminantes y espectros de radiación. Ya que el humo y la contaminación provocada principalmente por el Dióxido de azufre procedente del combustóleo que se quemaba en las industrias, el carbón que se usa en las carboeléctricas, y las emisiones de vehículos automotores, son la principal causa de la presencia del «smog fotoquímico» en las grandes ciudades como es el caso de la ciudad de México.
Palabras Clave: radiación, SOx, NOx, longitud de onda.
INTRODUCCION
La formación fotoquimica de los contaminantes atmosféricos, se estudia comumente en cámaras de ambiente controlado usando luz negra fluorescente que tiene algunas propiedades diferentes cuando se le compara con la luz natural. La técnica más usada en la medición de la luz ultravioleta en estudios fotoquimicos, es la irradiación de bióxido de nitrógeno (NO2) en atmósfera de nitrógeno.
Radiación solar: La radiación solar no solo calienta la atmósfera planetaria, es causante de los desequilibrios de la química atmosférica, debido a la iniciación de procesos químicos y consecuentemente a los cambios fotoquímicos primarios, es decir a los choques intermoleculares de las velocidades de reacción de toda la gama de contaminantes presentes.
METODOLOGÍA
Cambios fotoquímicos; La atmósfera está considerada como un reactor gigante, donde la fuente principal de calentamiento es el «sol» y la intensidad de luz que produce ha sido clasificada en regiones de radiación, de estas las más preocupante, son las regiones que corresponden a la región visible y la región ultravioleta que es donde se encuentran presentes fragmentos de constituyentes atmosféricos los cuales producen átomos, radicales, iones y partículas en estado de excitación.
Para fines de investigación el espectro solar se ha dividido arbitrariamente en intervalos que varían desde 290 y 700 nm.
Ya que a mayores longitudes de onda la absorción de la radiación es interferida por el vapor de agua y es en estos intervalos donde, se suceden todas las reacciones fotoquímicas que se encuentran como contaminantes de la atmósfera.
Tipos de Energía producidos en los procesos fotoquímicos primarios
Los tipos de energía más conocidos producidos en los procesos fotoquímicos primarios son:
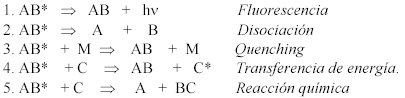
Los procesos fotoquímicos primarios y secundarios constituyen el mecanismo de todas las reacciones fotoquímicas; así los resultados de los cambios en las concentraciones iniciales, son variables dependientes del tiempo y han sido establecidas en base a los sistemas de ecuaciones de velocidad cinética de reacción.
A los sistemas primarios, se les trata como series de reacciones elementales tratamiento muy similar al de las reacciones térmicas elementales. La velocidad de una reacción debida a un cambio químico, es considerada como parte un proceso primario individual el cual puede cuantificarse de la siguiente forma:
En la atmósfera, se toma en cuenta la atenuación de la radiación solar que corresponde a los cambios de intensidad de las bandas espectrales divididas arbitrariamente y donde adicionalmente la dispersión de la radiación solar produce o presenta un componente difuso de flujo solar. Así la radiación directa del flujo y la radiación directa, son los causantes de los efectos fotoquímicos en las regiones espectrales del visible y ultravioleta la atenuación por absorción, es confinada a la estratosfera en el UV lejano.
Por ello en nuestros experimentos, es necesario considerar aquellas especies que absorben radiación solar en un rango de 3000-4000 Å (Fynlandson et al, 1998). Así los compuestos llamados contaminantes primarios (smog fotoquímico), absorben radiación cerca del ultravioleta incluyendo el dióxido de nitrógeno (NO2), los aldehídos y el dióxido de azufre (SO2).
A los compuestos anteriores se les ha considerado como precursores de la formación de contaminantes secundarios tales como: ozono, PAN’S, nitratos y nitritos de alkilo, etc., y son absorbidos en esta región espectral. Algunos autores (Seinfield y Hech, 1998) consideran a los contaminantes primarios como una función del espectro de absorción, de la concentración atmosférica, de la intensidad de la radiación solar y de la función de la longitud de onda acorde a la superficie de la Tierra.
Un adecuado conocimiento del flujo en la región espectral del ultravioleta (UV) es muy importante para el total entendimiento de la fotoquímica en la Estratosfera y la presencia del ‘smog » en el aire urbano. Así para realizar los cálculos de los coeficientes de fotodisociación de las especies químicas presentes en la atmósfera, se requiere una resolución espectral de 1 nm ya que coeficientes a mayores resoluciones espectrales nos involucran moléculas sujetas a predisociación por la estructura de las bandas de absorción la cual, se traslapa con las bandas espectrales, ejemplos de estas moléculas tenemos al oxígeno y el óxido nítrico.
DESCRIPCION DEL EXPERIMENTO
En los experimentos realizados en cámara de ambiente controlado en donde se simularon las condiciones atmosféricas, pudimos simulara y dividir el espectro del sol, en tres regiones de onda; a) <120 nm, b).120-300 nm, c).300-1000 nm. Estas bandas son las consideradas a una distancia de 100 km. Corresponden a la región del espectro ultravioleta lejano.
Por otro lado la radiación en la segunda región espectral 120-300 nm es la que corresponde a la estratosfera, y la radiación de longitudes de onda arriba de los 1000 nm no posee suficiente energía para una acción fotoquímica y no se le tomó en cuenta.
Aunque el nitrógeno, es uno de los más abundantes en la atmósfera no se le considera un buen absorbedor en regiones espectrales arriba de los 120 nm ya que su espectro a 145 nm es demasiado débil, los mayores absorbedores en la región espectral del ultravioleta, son el ozono y el oxígeno.
Una comparación directa de los efectos de la radiación artificial con la radiación natural, ha sido estudiada y gran cantidad de datos obtenidos en diferentes laboratorios con cámaras muy similares a la nuestra. (Cisniega, 1984; Altshuller, 1998)
Los experimentos de oxidación del óxido nítrico fueron conducidos por inyección de 80 % NO y 20 % NO2 a la cámara la cual previamente fue purgada con aire puro. El experimento se resguardó de la luz y se mantuvo en completa obscuridad durante el tiempo necesario para realizar y analizar los subproductos.
FORMACIÓN DE OZONO
La fuente de formación de ozono en la atmósfera es la fotólisis del NOx la cual procede vía la siguiente reacción:
![]()
seguido de la recombinación del triplete del oxígeno según:
![]()
y cuando el ozono se produce en la reacción (2), nosotros observamos que este reaccionó rápidamente con el NO, según observamos en la reacción 3. Sin embargo como ya se mencionó anteriormente el ozono no se detectó en nuestros experimentos.
![]()
la química de los óxidos de nitrógeno en la troposfera, es muy similar a la de aquellos óxidos presentes en atmósferas contaminadas de las grandes ciudades excepto que las concentraciones son relativamente pequeñas.
La disminución de ozono dentro de la cámara, ha sido reportado por Carter et al. (1996 ) como la vida media en el interior de esta, mientras que la reactividad, se utiliza para medir la formación del «smog» dentro de la cámara, y que la reducción en la vida media en condiciones de irradiación es debida a la formación de reacciones secundarias que son seguidas de la fotólisis de ozono. Las mediciones de vida media de los contaminantes en estudio, se realizaron en periodos que oscilaron desde 70 – 90 horas. La oxidación del NO, procede en completa obscuridad como consecuencia de una reacción térmica de tercer orden en ausencia de especies orgánicas acorde a la siguiente reacción.
![]()
La disminución en la concentración del NO por exceso de radiación así como el incremento en las velocidades de reacción se puede atribuir a la participación de contaminantes orgánicos en la fotoquímica de la reacción del NO de acuerdo a la ecuación 4.
CONCLUSIONES
El propósito de este estudio fue el desarrollo experimental para la medición del incremento de las reactividades relacionadas a la absorción en las diferentes bandas espectrales y la formación de ozono en la atmósfera. Las observaciones obtenidas concuerdan con los reportes de la literatura, nos demuestra que los incrementos en las reactividades del NO y de compuestos orgánicos dependen del mecanismo y la velocidad de la reacción. Así como el factor de magnitud en el que se incrementa la reactividad del NO que depende de cuanto NOx, está presente, este es el factor en el cual existe un proceso de decaimiento vibracional intermolecular con perdidas de energía a través de muchos procesos de colisión con otros de la misma molécula en estado basal o por colisiones con otros gases. El fenómeno se presenta como una serie de moléculas en estado de relajación, la cual o las cuales son desactivadas en el más bajo nivel vibracional del estado de excitación. Mientras que el proceso bimolecular (quenching) desactiva la o las moléculas para volverlas al estado basal. También se observó que en el proceso bimolecular la presencia de una molécula reactiva del oxígeno «fotodisociación» sé recombina con las reacciones «fotolíticas» de los productos primarios.
Observamos que todos estos procesos son lo suficientemente rápidos, compiten entre sí en cada nivel vibracional de o los estados excitados. Finalmente la foto-transformación del «quantum», hace posible la formación de varios procesos «fotoquímicos» como los observados en nuestros experimentos y en la contaminación del aire urbano de las grandes metrópolis.
BIBLIOGRAFIA
Altshuller, A.P., Lonneman S.L., (1998) Technique for measuring Photochemical reactions in atmospheric samples. Sc. & Technol. 4 , 6 ,506.
Atkinson, R. ; Carter W.P.L. At, Federal Register (1999) USA., Measurement of photochemical oxidants in the atmosphere. FR-41, No. 195. Atmosph. Chem. 1995, 3, 377- 405.
Carter, W.P.L.; Lurman, F.M.; Atkinson, R. Lloyd, A.C. (1996) Development and Testing of a surrogate Species Chemical
reactions Mechanism. EPA. USA. Research triangle Park, NY. EPA – 600/3-96-031.
Cisniega Rojas M.G., (1984) Ph. D. Thesis, University of London; England.
Fynlandson and Pitts, B.J. , Pitts J.N. Jr., (1998) Atmospheric Chemistry, Fundamnetals and experiemntal techniques, Wiley N.Y.
Seinfield, J.H. Hech, T.A., (1998) Existing needs in the experiemntal and chemical observational study of atmospheric chemical reactions.. EPA-RA-98-031.
Dra. Guadalupe Cisniega Rojas
Clemente Meza Rodríguez
Salvador Castillo Cervantes
Marina Morán-Pineda
XXVIII Congreso Interamericano de Ingeniería Sanitaria y Ambiental Cancún, México, 27 al 31 de octubre, 2002