Aplicación del Biopolímero Quitosano para la remediación de Efluentes Líquidos emulsionados provenientes de la industria petrolera
1. INTRODUCCIÓN
Los hidrocarburos obtenidos del petróleo son una de las fuentes de energía más importantes en la actualidad. El proceso de refinación utiliza grandes cantidades de agua en varias etapas del proceso generándose efluentes líquidos contaminados. Estos efluentes deben ser tratados para cumplir con las regulaciones ambientales y mejorar su calidad antes de ser volcados en cuerpos de agua adyacente a las plantas de refinación y petroquímica. En el caso de la provincia de Buenos Aires la concentración máxima admisible de hidrocarburos en el efluente debe ser menor a 30 mg/L (Resolución 336/2003-Privincia de Buenos Aires).
Los efluentes líquidos en una planta suelen encontrarse emulsionados requiriéndose su separación en sus dos componentes mayoritarios: agua y fase oleosa (petróleo y derivados).
Una de las estrategias con más frecuencia usada para la depuración de este tipo de contaminantes en las refinerías son las piletas API, en estas la separación de fases ocurre por diferencia de densidad, sin embargo es frecuente que los efluentes generados estén emulsionados siendo difícil su separación física, por ende actualmente exista la tendencia de utilizar coagulantes y floculantes que sean amigables y biocompatibles con el medio ambiente. Entre los procesos más económicos y sustentables se encuentra la utilización de biopolímeros que no generan barros tóxicos como subproducto del proceso de clarificación.
En este sentido y en el marco de nuestra participación del proyecto PIO UNLP-CONICET se propone como estrategia innovadora la utilización de biopolímeros que logren desestabilizar dichas emulsiones generando la clarificación del agua para su vertido. Los biopolímeros son ecológicamente compatibles, por ser biodegradables y no tóxicos.
El quitosano (QS) es un polisacárido lineal formado por cadenas de β-(1-4) D-glucosamina (unidades deacetiladas) y N-acetil-D-glucosamina (unidad acetilada). Este biopolímero se obtiene a partir de residuos sólidos de la industria pesquera como son caparazones de crustáceos, langostinos, etc. que presentan una cantidad apreciable de quitina (Q). Al desacetilar los grupos acetamida presentes en la Q se obtiene el QS, cuyas múltiples aplicaciones en alimentos, en el tratamiento de aguas, medicina etc., han sido documentadas. Es biodegradable, no tóxico y un agente coagulante/floculante. Su potencial como agente desestabilizante de emulsiones radica en que presenta grupos amino libres formando un polímero policatiónico que reacciona con las cargas negativas generando fenómenos de coagulación y floculación (Jayakumar y col., 2007). La composición y estructura del QS son muy similares a las de la celulosa; la diferencia es que el quitosano tiene un grupo amino primario en el carbono 2 del anillo de la hexosa.
Los objetivos de este trabajo fueron: (a) estudiar la acción del quitosano para la clarificación de aguas residuales de la industria del petróleo (b) analizar la capacidad desestabilizante del quitosano en solución y su poder clarificante en un sistema modelo constituido por emulsiones estables a partir de petróleo, agua y un tensioactivo aniónico biodegradable
(dodecilsulfato de sodio) (c) Determinar el tiempo mínimo para el cual se genera la floculación y precipitado de la fase oleosa (d) analizar el fenómeno de desestabilización mediante la medición de turbidez, demanda química de oxígeno (DQO), mediciones ópticas basadas en la dispersión estática de la luz y Potencial-Z.
2. PARTE EXPERIMENTAL
2.1 REACTIVOS Y COMPUESTOS QUÍMICOS
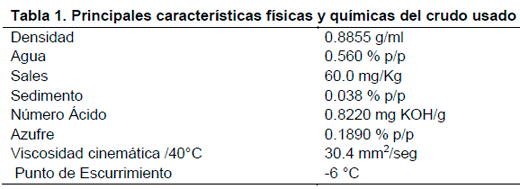
Los sistemas emulsionados con los que se trabajó se formularon a partir de: i) petróleo (crudo) procedente de la Patagonia Argentina; la caracterización de este material fue provista por Refinería YPF La Plata, y se describen en la Tabla 1, ii) agua potable y iii) como agente estabilizante dodecilsulfato sódico (SDS) el cual es un tensioactivo iónico de carácter aniónico. El Q en solución con una concentración de 0.5% p/v se preparó a partir de quitosano comercial marca Sigma con un grado de desacetilación > 85 %, el cual se disolvió en solución de ácido acético 1.5 % (v/v). Se escogió el SDS como emulsificante iónico en los sistemas debido a su alto grado de biodegradabilidad (Singer y Tjeedema, 1993).
 |
2.2 EMULSIONES O/W
Las emulsiones estudiadas contenían una concentración de 2550 ppm de petróleo, en agua destilada. Se analizaron dos tipos de emulsiones con y sin presencia de SDS. La concentración de agente tensoactivo fue de 35 mM. Los sistemas emulsionados se obtuvieron con equipo Ultra Turrax T-25 (Janke & Kunkel GmbH, Staufen, Germany) a velocidad de 13500 min-1 durante 5 minutos. La fase acuosa se preparó mezclando agua destilada y un agente tensioactivo aniónico biodegradable (SDS).
2.3 DEMANDA QUÍMICA DE OXIGENO (DQO)
Es un método aplicable en aguas continentales (ríos, lagos o acuíferos), aguas negras, aguas pluviales o agua de cualquier otra procedencia que pueda contener una cantidad apreciable de materia orgánica. La demanda química de oxígeno (DQO) se expresa en miligramos de oxígeno diatómico por litro (mgO2/l). La DQO se determinó utilizando un espectrofotómetro Hach DR 2800 (Loveland,Colorado, EEUU) a 620 nm, (Hach Método No.8000)
2.4 ESTUDIO DE LA DESESTABILIZACIÓN DE LAS EMULSIONES POR MÉTODO DE DISPERSIÓN ESTÁTICA DE LA LUZ
La desestabilización de las emulsiones se analizaron utilizando un Instrumento basado en el fenómeno de dispersión estática de la luz denominado Turbiscan; para este fin se usó un analizador óptico vertical de barrido QuickScan (Beckman Coulter; Fullerton, USA): Este es un instrumento capaz de analizar la estabilidad de sistemas coloidales y dispersiones concentradas, mediante la medición de la transmitancia y la retrodispersión (Backscattering (BS)) de un sistema atravesado por un pulso de luz correspondiente al infrarrojo cercano. La muestra a ser analizada está contenida en un tubo o celda de vidrio, colocado cerca de una cabeza lectora compuesta por una fuente de luz IR-cercano (λ= 850 nm) (Mengual y col., 1999). El equipo permite hacer varias mediciones a diferentes tiempos, obteniéndose una serie de perfiles de retrodispersión (backscattering) en función del tiempo (Pan y col., 2002)
2.5 TURBIDEZ RESIDUAL
Se calculó la densidad óptica (D500) de la emulsión con y sin agregado de quitosano a 500 nm usando Espectrómetro UV-VIS 1240 (Shimadzu Corporation, Kyoto, Japón). El % turbidez residual (TR) se obtiene con la Ecuación 1.
 |
2.6 POTENCIAL Z
Se midió el potencial Z de las siguientes soluciones a) emulsión petróleo/agua b) emulsión con agregado de quitosano con dosaje óptimo (máxima clarificación del efluente) y c) emulsión con agregado de quitosano en exceso (sobredosificación) utilizando un equipo Zeta Potential Analyzer 90Plus/Bi-MAS (Brookhaven Instruments Corporation, Holtsville, NY, USA). La medida del potencial Z consiste en determinar la carga en la superficie externa del coloide (Capa Stern, basándose en la teoría de la doble capa eléctrica). El potencial zeta permite conocer el comportamiento del coloide (movilidad electroforética) durante diferentes condiciones del proceso (pH, concentración y tipo de sales).
3. RESULTADOS Y DISCUSIÓN
3.1 DISTRIBUCIÓN DE TAMAÑOS DE PARTÍCULAS Y DQO DE LA EMULSIÓN FORMADA
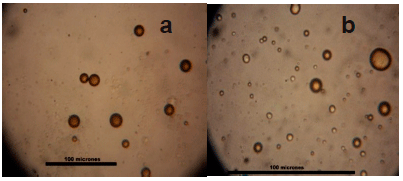
Teniendo en cuenta las características para la elaboración de la emulsión (O/W) en la Fig.1 a y b se muestra las micrografías obtenidas de la emulsión petróleo/agua estable. El diámetro promedio de la partícula dependiente del volumen (D [4,3]) fue de 13.13 (0.07) μm, los valores entre paréntesis corresponden a la desviación estándar Para la emulsión O/W con SDS se obtuvo una DQO de 6442 (399) mg/L, los valores entre paréntesis corresponden a la desviación estándar. El DQO de la emulsión estable (O/W) no cumple con la normativa de la autoridad nacional del agua ya que la resolución 336/2003 establece que la DQO para la descarga de efluentes en conductos pluviales y cuerpos de agua superficiales debe ser ≤ 250 mg/L y en mar abierto ≤ 500 mg/L, por lo tanto establecer una estrategia para la reducción de la DQO es importante.
|
Fig. 1 Micrografías obtenidas de la emulsión estable O/W (Petróleo/agua) obtenidas con |
3.2 DESESTABILIZACIÓN DE LOS EFLUENTES EMULSIONADOS POR ADICIÓN DE QUITOSANO
En todos los casos el agregado de quitosano generó una desestabilización de la emulsión que se inició prácticamente de manera instantánea requiriendo un tiempo mínimo de 3 horas para alcanzar una separación/sedimentación completa de la fase acuosa y oleosa. En la Fig. 2 se muestra la acción clarificante del quitosano en emulsiones estabilizadas con SDS. Se comparó un control (emulsión sin quitosano) con varias emulsiones donde se fue incrementando la dosis de quitosano observando su acción como coagulante después de 5 horas de tratamiento. La emulsión desestabilizada genera un flóculo que posteriormente sedimenta. Si la dosis es la óptima (Fig. 2c) se distingue una interfase que separa la zona acuosa clarificada y el flóculo oleoso que sedimenta. Esto ocurre debido a la aglomeración de las gotas por mecanismos de neutralización de carga superficial correspondiente a la interacción del tensioactivo aniónico (SDS) con el quitosano. Por otro lado si la dosis de quitosano es insuficiente (Fig. 2a-b) la formación del fenómeno de coagulación es incompleto debido a que la cantidad de cargas positivas aportadas por el quitosano son insuficientes para neutralizar las moléculas iónicas del SDS cargadas negativamente que estabilizan la emulsión.
En la Fig. 2d se observa el efecto de la sobredosificación de quitosano; en la fase acuosa superior existe una región turbia en comparación con la Fig. 2c, además del precipitado negro. En este caso aunque exista una desestabilización de la emulsión con el consiguiente precipitado un aumento excesivo de quitosano puede generar una repulsión entre micelas positivas provocando una parcial re-estabilización de las partículas O/W. Este efecto es no deseable (Pinotti y col., 2001; Rodríguez y col., 2002) por ello es necesario detectar la dosis óptima.
|
Fig. 2. Efecto de las dosis de quitosano después de 5 horas en la desestabilización de las emulsiones petróleo/agua con presencia de SDS; las imágenes mostradas de izquierda a derecha corresponden: Control (emulsión sin quitosano) y emulsiones con diferentes dosis de quitosano: a) 50 mg/L, b) 100mg/L, c) 500mg/L, d) 830mg/L En la Fig. 3 se muestra el porcentaje de turbidez residual (%TR) en relación al volumen agregado de quitosano. Se puede observar el valor mínimo de la curva correspondiente a una dosis óptima de quitosano agregado (mínimo %TR). |
|
Fig. 3 Efecto de la dosis agregada de la solución floculante conteniendo quitosano (mg |
3.3 ANÁLISIS DE LA DESESTABILIZACIÓN DE LA EMULSIÓN UTILIZANDO UN MÉTODO ÓPTICO
La evolución de los perfiles del %BS se muestra en la Fig. 4. La Fig. 4a corresponde a la emulsión sin agregado de quitosano (control) ésta presenta una alta estabilidad global y los perfiles de %BS no varían en la celda durante todo el período de tiempo estudiado. En contraste en las Fig. 4b y c, que corresponden a emulsiones con SDS desestabilizadas por el agregado de quitosano, el %BS presenta un salto en la interfase flóculo oleoso y zona clarificada, siendo esta zona una interfase móvil que se aproxima a la zona inferior del tubo a medida que transcurre el proceso de floculación y posterior sedimentación. En el caso de utilizar quitosano en exceso en la Fig. 4b se observa el mismo fenómeno pero con mucha menor intensidad y menor clarificación (menor valor de BS%).
|
|
3.4 POTENCIAL Z
Se obtuvo el potencial Z de la emulsión estable sin agregado de quitosano y del sobrenadante (región clarificada) producto de la desestabilización a dos dosis diferentes (dosis óptima y mayor que la óptima). En el caso de la emulsión estable original (sin agregado de quitosano) el potencial resultante fue de -85.35 (1,59) mV (en paréntesis desviación estándar), esto se debe a la presencia del surfactante iónico usado para estabilizar la emulsión. Cabe señalar que un valor absoluto alto de potencial Z indica que la emulsión es estable debido a la repulsión entre las gotas cargadas eléctricamente .
Una vez que se agregó quitosano para desestabilizar la emulsión el potencial Z para la región clarificada disminuyó en valor absoluto siendo de -0.3 (0.2) mV lo cual indica la neutralización de cargas del sistema. Por otra parte el potencial Z de la emulsión con exceso de quitosano cambió de signo resultando positivo (21.09 (0.35) mV), debido a la parcial reestabilización de la emulsión causada por la repulsión entre cargas positivas.
4. CONCLUSIONES
Se logró comprobar la acción del quitosano como coagulante/floculante en sistemas emulsionados con presencia de petróleo determinando cual es la dosis adecuada para alcanzar una fase acuosa final con un mínimo de turbidez. El quitosano al ser un biopolímero con propiedades de polielectrolito catiónico tiene un alto poder de acción para generar una separación de fases óptima. Cabe señalar que la clarificación de la fase acuosa se logra en tiempos mínimos de contacto de quitosano con el efluente del orden de 3 horas permitiendo que se cumpla con los requerimientos para el vertido en cuerpos de agua adyacentes a la refinería. Asimismo es importante recalcar que este biopolímero es compatible con el medio ambiente y proviene de subproductos residuales de la industria pesquera Argentina, por lo tanto su uso resulta en una alternativa sustentable.
BIBLIOGRAFÍA
Jayakumar, R., Nwe, N., Tokura, S., y Tamura, H. (2007). Sulfated chitin and chitosan as novel biomaterials. International Journal of Biological Macromolecules, 40(3), 175-181.
Mengual O, Meunier G, Cayré I, Puech K y Snabre P (1999). Turbiscan MA 2000: multiple light scattering measurement for concentrated emulsion and suspension instability analysis.
Talanta, 50 (2),445-456.
Pan, L. G., Tomás, M. C., y Añón, M. C. (2002). Effect of sunflower lecithins on the stability of water-in-oil and oil-in-water emulsions. Journal of surfactants and detergents, 5(2), 135- 143.
Pinotti, A., Bevilacqua, A., y Zaritzky, N. (2001). Comparison of the performance of chitosan and a cationic polyacrylamide as flocculants of emulsion systems. Journal of Surfactants and Detergents, 4(1), 57-63.
Rodríguez, M. S., Albertengo, L. A., y Agulló, E. (2002). Emulsification capacity of chitosan.
Carbohydrate polymers, 48(3), 271-276.
Singer, M. M., y Tjeerdema, R. S. (1993). Fate and effects of the surfactant sodium dodecyl sulfate. Reviews of environmental contamination and toxicology (pp. 95-149). Springer New York.
Por: Pérez-Calderón, John (1), Santos, María Victoria (1-2), Zaritzky, Noemí (1-2)
(1) Centro de Investigación y Desarrollo en Criotecnología de Alimentos, CONICET, CICPBA, Argentina, Universidad Nacional de La Plata.
(2) Depto. de Ingeniería Química- Facultad de Ingeniería, Universidad Nacional de La Plata, Argentina
Fuente: Quimica
4º Jornadas ITE – 2017 – Facultad de Ingeniería – UNLP