Combustión
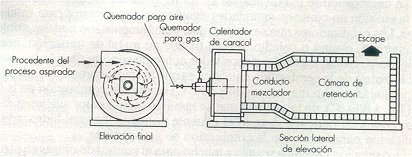
La combustión implica el tratamiento de los contaminantes del aire del hidrocarburo combustible y del monóxido de carbono mediante su oxidación completa a dióxido de carbono y agua. En algunos casos está presente una cantidad de hidrocarburo para soportar la combustión sin material combustible extra. En este caso, el material simplemente se transfiere dentro de una cámara de combustión diseñada para este propósito (ver figura) y los gases se tratan como gases combustibles ordinarios, los cuales por lo general se queman tras premezclarse con aire (como en un mechero de Bunsen).
Las cámaras se diseñan para mantener los gases a 700ºC durante cerca de medio segundo; en la práctica se ha encontrado que este tiempo es suficiente para una combustión completa. Si hay una energía térmica insuficiente en los hidrocarburos de la corriente de gas, se suministra material combustible adicional, el cual puede quemarse por separado o, en el caso del gas, mezclarse con el gas de desecho contaminado.
En las fábricas grandes, donde hay calderas de vapor, algunas veces es posible transferir los gases de desperdicio que contienen al contaminante hacia lla cámara de combustión de la caldera; sin embargo, a menos que la caldera se haya diseñado específicamente para esta tarea adicional, pueden surgir problemas severos. Por ejemplo, si los gases de desecho contienen sulfuros orgánicos, la oxidación de éstos puede originar cantidades grandes de dióxido y trióxido de azufre, así como guiar a corrosión y deterioro rápido de la caldera. Los gases de desecho que contienen cantidades apreciables de vapor de agua, el cual tiene un calor específico elevado, pueden reducir la temperatura de la caldera y afectar así su funcionamiento.
Si hay oleadas en la concentración de gas, en composición y cantidad, la combustión se vuelve difícil. Bajo tales circunstancias, las cuales son comunes en las refinerías de petróleo, se utilizan llamaradas especiales que tienen luces piloto y combustible suplementario. Ya que estas llamaradas queman cantidades considerables de compuestos aromáticos (anillos orgánicos) los cuales producen una flama humeante, hay una provisión especial para la inyección de aire en exceso y vapor, los cuales reaccionan con el carbono no quemado en la flama y producen monóxido de carbono e hidrógeno:
C + H2O ® CO + H2
H2 + ½O2 ? H2O
CO + ½O2 ? CO2
En total C + O2 ? CO2
De esta manera, la combustión sin humo se realiza y la llamarada controlada es apenas visible.
La combustión se puede auxiliar en forma catalítica en circunstancias en que la emisión no contiene cantidades significativas de venenos para catalizadores. Los catalizadores que se utilizan más comúnmente son metales nobles; por ejemplo, platino o paladio, o bien óxidos de metal de transición como manganeso, cromo o cobalto depositados sobre un soporte de alúmina poroso. La ventaja de la combustión catalítica es que los hidrocarburos se oxidan a temperaturas mucho menores (400ºC a 500ºC) que las de la combustión en la flama (700ºC a 800ºC), de tal manera que se requiere menos calor adicional. Esto es en particular beneficioso cuando el efluente contiene material hidrocarburo insuficiente para hacer que la combustión se autosustente.
La oxidación catalítica se utiliza mucho para el control de olores en el procesamiento de alimentos, por ejemplo, en el tostado de café, y para la oxidación de vapores orgánicos del horneado y esmaltado de pinturas; ambos procesos tienen emisiones bajas de venenos potenciales de catalizadores