Eliminación de 2-clorofenol de soluciones acuosas mediante algas marinas: evidencias de mecanismo de adsorción
RESUMEN
Se investigó el mecanismo por el cual las algas marinas Bory y Bory remueven 2-clorofenol a partir de soluciones acuosas mediante experimentos de adsorción discontinuos y técnicas instrumentales. Se evaluó el efecto de la presencia de iones metálicos en el proceso de adsorción. Los resultados indican que el plomo aumenta ligeramente la adsorción de 2-clorofenol. Esto sugiere dos diferentes mecanismos de adsorción de ambos tipos de contaminantes por ambas algas marinas y un posible efecto sinérgico entre ellos. Análisis de microscopía electrónica de barrido electrónico complementado con análisis de rayos X por energía dispersiva indicaron una adsorción predominantemente de superficie. Finalmente, se determinó el cambio en la energía libre de Gibbs (∆G0 ) del proceso, concluyendo que la adsorción no es espontánea para ninguna de las algas estudiadas, lo cual corrobora la ausencia de interacciones electrostáticas y la existencia de interacciones poco polares en un ambiente desfavorable rodeado de grupos hidroxilo.
Palabras clave: Algas marinas, 2-clorofenol, energía libre de Gibbs, plomo, biosorción.
INTRODUCCIÓN
La contaminación de fuentes hídricas por sustancias orgánicas e inorgánicas ha sido siempre de preocupación mundial. Entre las típicas sustancias orgánicas consideradas tanto como subproductos no deseados y materia prima en numerosas industrias, están los fenoles 1.
Fenoles, sus derivados y aquellos compuestos orgánicos que contienen anillos aromáticos condensados pertenecen al grupo de contaminantes más tóxicos y comunes de la industria de plásticos, tintes y papel. La biodegradación de ácidos húmicos, taninos y ligninas también producen fenoles. Estos compuestos son tóxicos y se sospecha su efecto carcinógeno en humanos. Por esta razón, un gran número de fenoles han sido listados en la European Community Directive y en laUS Environment ProtectionAgency (EPA).
La presencia de fenoles en medios acuáticos causa cambios en las propiedades químicas (pH, demanda de oxígeno, alcalinidad, oxígeno disuelto, etc.), físicas (olor, sabor, color, viscosidad, turbidez, temperatura, etc.) y biológicas, dañando la calidad de agua para el uso humano y originando disturbios en el equilibrio ambiental.
Los clorofenoles son productos secundarios típicos en industria del papel durante la fase de blanqueamiento, así como en la preparación de antisépticos y pesticidas.Además, son ácidos permeables a la piel humana y son rápidamente absorbidos por el tracto gastro-intestinal. La intoxicación por clorofenoles causa aceleración de a respiración, vómitos y náuseas en humanos2. Estos compuestos fenólicos son generalmente eliminados mediante técnicas convencionales como coagulación, extracción por solventes, adsorción por carbón activado, intercambio iónico con resinas, degradación fotocatalítica en suspensiones de dióxido de titanio, oxidación por peróxido de hidrógeno, biodegradación, entre otras3-7.
En las últimas décadas, la biotecnología ha abordado el problema de la contaminación ambiental mediante el desarrollo de tecnologías limpias para la remoción de contaminantes orgánicos e inorgánicos. La biosorción ha constituido un arma eficiente, de bajo costo y de fácil aplicación para la destoxificación de aguas residuales provenientes de industrias y minas contaminadas con metales pesados 8, obteniendo resultados positivos. Los biosorbentes comúnmente empleados son algas marinas 9, hongos comestibles01, levaduras 11y otros 12-14.
Por otro lado, Perú es conocido por su diversidad de recursos naturales. Las algas marinas yacen en las playas sin ningún beneficio, siendo al contrario preocupación de municipios y de la comunidad. Por esta razón, dos variedades de algas marinas del litoral peruano fueron escogidas para la eliminación de compuestos fenólicos en estudios previos16 .
El uso de algas marinas en la eficiente remoción de 2-clorofenol (2-CP) ya ha sido demostrado anteriormente15-16 por nuestro grupo de investigación. Otros grupos de investigación han empleado cascarón de huevo, desechos municipales tratados, corteza de coco, plumas de aves de corral, etc.; pero muy pocos han propuesto un mecanismo de adsorción coherente con los resultados experimentales.
Además, la presencia simultánea de compuestos orgánicos e inorgánicos en las aguas residuales marca un reto en el uso de biosorbentes que se ajusten con mayor precisión a un agua de desecho real. La presencia de plomo como modelo de contaminante inorgánico nos permitirá determinar si el proceso de adsorción de 2-CP es sinérgico, aditivo, competitivo o indiferente respecto al plomo.
PARTE EXPERIMENTAL
Soluciones y reactivos
Soluciones stock de 1000 ppm fueron preparadas disolviendo 2-clorofenol (grado analítico, MERCK) en 1 L de agua desionizada. Se prepararon diferentes soluciones por dilución del stock hasta alcanzar la concentración deseada. Todas las diluciones fueron preparadas con agua tipo I, purificada por ósmosis reversa mediante un purificador Barnstead/Thermolyne (Dubuque IA) D2714, el cual proporciona agua con una máxima conductividad de 18 mΩ.
El pH inicial de cada solución fue ajustado al valor óptimo añadiendo alícuotas de 0,1N HCl y 0,1N NaOH antes de ponerse en contacto con el adsorbente. No se observaron cambios significantes en el pH inicial luego de alcanzarse el equilibrio, por lo que se asumió un pH constante durante todo el proceso.
Adsorbentes
Las algas marinas Lessonia nigrescens Bory (A1) y Macrocystis integrifolia Bory (A2) fueron recolectadas de las playas de Tacna y Marcona en Perú, respectivamente, a una distancia aproximada de 200 m de la orilla. Las algas fueron lavadas con abundante agua potable, llevadas al laboratorio para su identificación taxonómica y mantenidas bajo refrigeración.
Luego, se lavó las algas con agua tipo I, secadas a temperatura ambiental, molidas, separadas de acuerdo a su tamaño de partícula mediante tamizado y almacenadas en un desecador hasta su uso.
Caracterización del adsorbente
Con el propósito de elucidar el mecanismo de adsorción de 2-CP en las algas marinas, se estudió la textura superficial y morfología de ambos adsorbentes mediante Microscopía de Barrido Electrónico (SEM) y Espectrometría de Rayos X por Energía Dispersiva (EDX) usando un Philips ESEM XL-30 TMP. Previo al análisis, la superficie de las muestras fue cubierta con una fina y eléctricamente conductiva capa de oro.
Efecto de la presencia de Pb(II)
Se estudió la interferencia de iones metálicos como adsorbatos competitivos de 2-CP por los sitios activos de los biosorbentes. Se consideró los mismos valores óptimos y se realizaron pruebas a diferente concentraciones de nitrato de plomo II (grado analítico, MERCK) en el rango 0 – 40 ppm.
Se realizaron experimentos discontinuos por duplicado evaluando el efecto de la presencia de iones metálicos en un agitador orbital INNOVA modelo 2100 a temperatura ambiente. Se mantuvo bajo una agitación de 200 rpm durante 24 h para asegurar el equilibrio. Las muestras fueron luego filtradas y se determinó la concentración residual de 2-CP mediante un espectrofotómetro UV-visible SHIMADZU modelo UV-mini 1240 a una longitud de onda de 274 nm.
Análisis de datos
Con el solo propósito de comparar el efecto de plomo en la adsorción de 2-CP por ambas algas marinas, la cantidad adsorbida de 2-CP se expresó como porcentaje de adsorción (% adsorción); calculado según la siguiente ecuación:
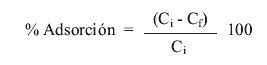 |
Donde Ci y Cf son las concentraciones inicial y en el equilibrio, respectivamente, de 2-CP expresadas en mg/L.
RESULTADOS Y DISCUSIÓN
Estudios previos mostraron mediante FTIR, que las algasA1 y A2 contienen grupos carboxilo, sulfonato, hidroxilo y amino en su estructura. Asimismo, se estudiaron las propiedades ácidobásicas de ambas algas 17 , determinándose una constante de ionización aparente de alrededor de 2,5. Estos estudios elucidaron los posibles centros de adsorción de fenoles e iones metálicos. Con el propósito de ampliar el conocimiento del mecanismo de adsorción de fenoles en algas marinas, se evaluó al algaA1 por SEM y EDX análisis, antes y después de ser puesto en contacto con 2-CP.
 |
Caracterización del adsorbente
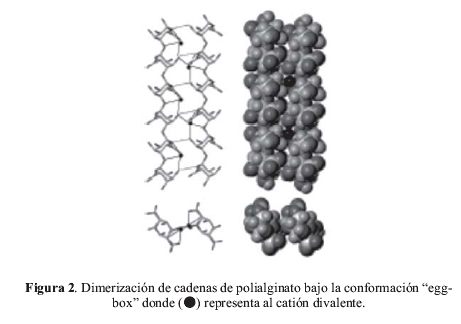
La figura 1a y 1b muestra el análisis SEM de A1 antes de la adsorción de 2-CP, observando una buena organización de la superficie, siendo capaces de reconocer estructuras helicoidales, confirmando la teoría del “egg-box” de los alginatos. Esta particular estructura pertenece exclusivamente a polialginatos y pectinas, los cuales son polisacáridos lineales. En el caso de los polialginatos, éstos se componen por unidades de ácidos (1,4) β – D – mamurónico (M) y α – L- gulurónico (G), distribuidos de forma no arbitraria, coexistiendo las secuencias MM, GM, GG y MG en el polímero. Estas cadenas se asocian formando dímeros, con la ayuda de cationes divalentes, en especial de iones calcio (II) (figura 2).
Los cambios producidos en la superficie de A1 causados por la adsorción de 2-CP se muestran en la figura 1c y 1d. Comparando las microscopías de menor resolución (x80), se nota una disminución de la porosidad del adsorbente, atribuyéndose a la deposición de 2-CP a nivel superficial, el cual llena las cavidades porosas del adsorbente. Por otro lado, a una resolución de x1274, la conformación egg-box ya no es tan fácilmente observable debido a la adsorción de 2-CP en el exterior del dímero de alginato.
 |
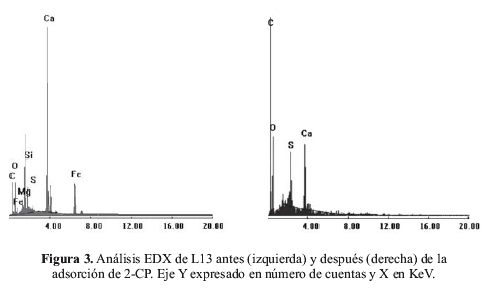
El estudio de microscopía electrónica fue verificado mediante análisis EDX, el cual se muestra en la figura 3. De los resultados, se observa un incremento de la cantidad de oxígeno y carbono en la superficie de A1 luego de la adsorción de 2-CP. Como se esperaba, la cantidad de carbono es mucho mayor comparada a la de oxígeno debido a la mayor composición en carbono de 2-CP. Este aumento en carbono mostrado por el análisis EDX confirma el llenado de poros del adsorbente por 2-CPque se observó en las microscopías de barrido electrónico.
 |
Efecto de la presencia de Pb (II)
La figura 4 muestra el efecto que produce la presencia de plomo divalente en la adsorción de 2- CP. Para ambas algas marinas, la presencia del ion Pb (II) no afecta notablemente la adsorción de 2-CP. Variando la concentración de plomo divalente entre 5 y 40 mg/L; el porcentaje de adsorción de 2-CP experimenta un ligero incremento. Esto se debe a que la adsorción de 2-CP y de cationes divalentes no compite por los mismos sitios de adsorción de algas marinas.
Como se explicó anteriormente, los metales pesados divalentes desplazan a los iones calcio (II) de la cadena polimérica tipo “egg box”, mientras que los compuestos fenólicos, en general, y entre ellos 2-CP, interacciona con los grupos hidroxilo mediante distintas fuerzas de atracción intermoleculares, entre ellas dipolo-dipolo y puentes de hidrógeno.
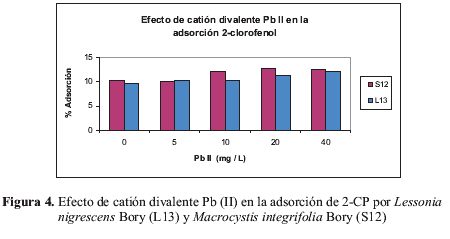 |
Como se observa en la figura 2, los grupos hidroxilo se ubican al exterior de la cadena polimérica de alginato, por lo que ambos mecanismos de adsorción son independientes y al contrario, la presencia de plomo como estabilizador de la conformación “egg-box” expone permanentemente a los grupos hidroxilo en la superficie del polímero para su interacción con 2-CP. Esto podría explicar el ligero incremento en el % adsorción de 2-CP a altas concentraciones de plomo de ~10% en ausencia de plomo a ~12% con 20 y 40 mg/L de Pb (II).
Finalmente, cabe resaltar que el%adsorción de 2-CP es idéntico con concentraciones de 20 y 40 mg/L de Pb(II), por lo que se puede postular que 20mg/L de Pb (II) seria la condición mínima para la estabilización de la conformación “egg-box” que permite la máxima adsorción de 2-CP.
Cálculo de la energía libre de Gibbs
De acuerdo a Sawalha et al.18 , la constante de adsorción en el equilibrio (kc) para la biosorción de contaminantes se calcula de la pendiente de la gráfica qe versus ce, utilizando la siguiente ecuación:
|
|
Estudios previos de nuestro grupo de investigación 15 , demostraron los parámetros óptimos de equilibrio de adsorción de 2-CP con los mismos adsorbentes, pero quedó pendiente la determinación de la espontaneidad del proceso. Para ello, se usaron los mismos datos experimentales para obtener la constante kc , como se muestra en la figura 5.
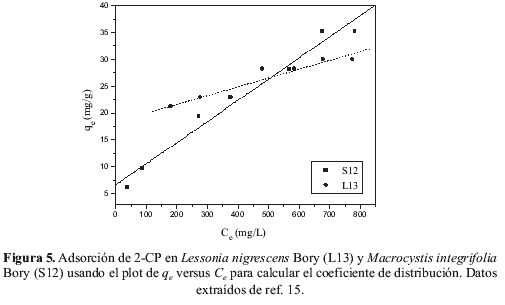 |
Luego, el cambio de la energía libre de Gibbs ΔG0 (kcal/mol) para la adsorción de 2-CP en ambas algas marinas se calculó mediante la siguiente ecuación:
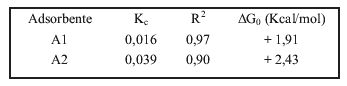
donde T es la temperatura en Kelvin y R es la constante universal de los gases (1,987 cal/mol.K). Los valores de kc y ΔG0 se muestran en la tabla 1.
De los resultados, se concluye que la adsorción no es espontánea con ninguno de los dos adsorbentes, lo cual corrobora la ausencia de interacciones electrostáticas entre 2-CP y las algas marinas sino, más bien, la existencia de interacciones poco polares en un medio adverso, que lo constituyen los grupos hidroxilos.
Tabla 1. Energía Libre de Gibbs para la adsorción de 2-CP en A1 y A1 a 25°C
CONCLUSIONES
Los resultados de este estudio muestran que la adsorción de 2-clorofenol (2-CP) en las algas marinas Lessonia nigrescens Bory (A1) y Macrocystis integrifolia Bory (A2) es un fenómeno netamente de superficie. La técnica instrumental de microscopía de barrido electrónico muestra una disminución en la porosidad del adsorbente luego de la adsorción de 2-CP debido a la deposición o agregación de 2-CP en la superficie del adsorbente. Esto fue corroborado mediante análisis EDX, el cual mostró un aumento en el contenido de oxí geno y carbono en la superficie del adsorbente luego de la adsorción de 2-CP. La presencia de plomo durante la adsorción de 2-CP causo un ligero aumento en el porcentaje de adsorción. Este resultado se vincula con la no competencia de ambos adsorbatos por los mismos centros activos, y al contrario, muestran cierto sinergismo estabilizando la conformación “egg-box” de los polialginatos. Finalmente, se observó un positivo cambio en la energía libre de Gibbs para ambas algas marinas, sugirieron además de la no espontaneidad del proceso, la ausencia de interacciones electrostáticas y la existencia de interacciones poco polares en un ambiente rodeado de grupos hidroxilo.
AGRADECIMIENTOS
Los autores deseamos agradecer al Consejo Nacional de Ciencia y Tecnología del Perú (CONCYTEC), al Fondo Concursable de Apoyo a la Investigación en la UPCH y al Departamento de Química de la Universidad Peruana Cayetano Heredia por el financiamiento para la realización del presente trabajo. Asimismo, expresamos nuestra especial gratitud a María Sun Kou por su seguimiento y asesoramiento en esta investigación.
REFERENCIAS
- Mbui D, Shiundu P, Ndonye R, Kamau GJ. Environ. Monit. , 2002, 4, 978-984.
- Farell J, Hunt S. Environmental Toxicology: Organic Pollutants, 1st edition, Ellis Horwood, England, 1998.
- Taman H, Okazaki M. Colloid Interface Sci., 1996, 179, 181-187.
- Haghseresth F, Nouri S, Lu G.Langmuir , 2002, 18, 1574-1579.
- Kilduff J, King C.Ind. Eng. Chem. Res. , 1997, 36, 1603-1613.
- Ramos N, GarcíaA, Molina Chem. Pap. . , 2005, 59, 161-165.
- LiY,YouY, Lien E.Arch. Environm. Conam. Toxicol. , 1999, 37, 427-430.
- Cuizano N, Navarro A. An. Quím. , 2008, 104, 120-125.
- NavarroA, Blanco D, Llanos B, Flores J, Maldonado H.Rev. Soc. Quím. Perú , 2004, 70, 147-157.
- Ramos K, Llanos B, Maldonado H, Navarro A. An. Quím., 2007, 103, 36-40.
- Wang J, Chen C.Biotechnol. Rev. , 2006, 24, 427-451.
- Rojas G, Silva J, Flores J, Rodriguez A, Ly M, Maldonado H.Sep. Purific. Technol. , 2005, 44, 31- 36.
- Miretzky P, SaraleguiA, Cirelli A.Chemosphere , 2006, 62, 247-254.
- SaeedA,Waheed-Akhter M, Iqbal M K.Sep. Purif. Technol. , 2005, 45, 2531.
- Navarro A, Cuizano N, Portales R, Llanos B.Sep. Sci. Technol. , 2008, 43, 3183-3199.
- Navarro A, Cuizano N, Lazo J, Sun-Kou M, Llanos B.J. Hazard. Mater. , 2008, en prensa.
- Cuizano N, Llanos B, Chang L, Navarro A.Rev. Soc. Quím. Perú , 2007, 73, 85-93.
- Sawalha M, Peralta-Videa J, Romero-Gonzalez J, Gardea-Torresday J.Colloid Interface Sci., 2006, 300, 100-104.
Por: Norma A. Cuizano a , Bertha P. Llanos a , Abel E. Navarro b
a – Departamento de Química, Facultad de Ciencias y Filosofía, Universidad Peruana Cayetano Heredia, Lima 31, Perú.
b – Department of Chemistry, Graduate School of Arts and Science, NewYork University, USA.
Fuente: Rev. Soc. Química Perú. 75 (2)