Catalizadores para la combustión de material particulado emanado de combustibles diesel y biodiesel
INTRODUCCIÓN
Los motores de combustión interna constituyen una de las principales causas de contaminación ambiental. En el caso particular de los motores diesel los principales contaminantes son las partículas de hollín o material particulado y los óxidos de nitrógeno.
El desarrollo de materiales catalíticos activos para la eliminación de contaminantes de gases de escape de motores diesel, ha sido motivo de un intenso trabajo de investigación en los últimos años. La eliminación de hollín proveniente de escapes de motores diesel, es un problema para el cual aún no se ha encontrado una solución completamente satisfactoria. Se debe lograr un sistema de filtrado eficiente, que retenga las partículas de muy pequeño tamaño generadas en el motor, evitando aumentos en la pérdida de carga del sistema de exhaución por taponamiento del filtro. Una de las opciones más adecuadas es que se autorregenere por combustión catalítica del hollín. Para esto, el catalizador debe tener actividad suficiente a la temperatura de los gases de escape.
En trabajos previos de nuestro grupo de trabajo se reportaron resultados obtenidos con catalizadores basados en potasio y cobalto, soportados en MgO, CeO2, y La2O3 (1-3). Se encontró que el catalizador K/La2O3 es una opción promisoria para la eliminación del hollín. Este catalizador en mezcla mecánica con el hollín presenta un máximo en el perfil de oxidación a temperatura programada entre 350 y 400°C. Esta temperatura de quemado de hollín se ajusta bien a los niveles térmicos disponibles en el escape de motores de carga pesada, y se acerca a los niveles térmicos disponibles en el escapes de motores de carga liviana.
El SO2, inevitablemente presente entre los productos de la combustión de cualquier combustible derivado del petróleo, constituye un problema en cuanto a que éste desactiva el catalizador. Si bien las futuras legislaciones se están haciendo progresivamente más estrictas en cuanto a los contenidos de material particulado y NOx , también lo están haciendo con respecto al contenido de azufre de los combustibles, lo cual constituye un aspecto sumamente positivo teniendo en mente la desactivación de los catalizadores frente al SO2.
La preparación del catalizador soportado en el filtro o monolito cerámico presenta inconvenientes adicionales. Se debe lograr un depósito con la composición previamente optimizada, que presente buena adherencia al soporte y que sea mecánica y térmicamente estable.
Finalmente, el estudio de las emanaciones de los biocombustibles, como el biodiesel, constituye un nuevo desafío, teniendo en cuenta que las actuales legislaciones en determinados países (y futuras en otros), están demandando el uso de porcentajes de éstos biocombustibles en mezcla con los combustibles tradicionalmente usados.
El objetivo de este trabajo es evaluar la actividad del catalizador K/La2O3 para la combustión de material particulado emanado por combustibles diesel. Se analiza la estabilidad del catalizador frente al SO2. También se analiza la estabilidad mecánica y térmica cuando se deposita el catalizador sobre un monolito cerámico, del tipo de los usados comercialmente.
Por último se compara la actividad del catalizador frente a la combustión de material particulado emanado por combustibles diesel y biodiesel.
La actividad de los catalizadores en polvo se evalúa mediante la técnica de oxidación a temperatura programada, en la cual, una mezcla mecánica de catalizador con hollín se somete a un proceso de calentamiento en corriente de O2 en N2.
Para analizar la estabilidad del catalizador frente al SO2 se somete el mismo a una corriente de 1000 ppm de SO2. Esta concentración de SO2 es extremadamente alta con respecto a las concentraciones presentes en el escape, pero se usa buscando desactivar rápidamente al catalizador. Con el propósito de regenerar al catalizador así envenenado, se usa la técnica de reducción a temperatura programada, en la cual, el catalizador se somete a un proceso de calentamiento en una corriente de 5% de H2 en Ar. Para analizar la capacidad de adsorción de NOx del catalizador se somete el mismo a un proceso de calentamiento en una corriente de NO y O2. Las especies presentes en el catalizador se caracterizan mediante la técnica de Espectroscopía de Infrarrojo.
Como una aproximación al comportamiento real del catalizador en el escape del motor, se estudia la preparación de catalizadores de K/La2O3 soportados en monolitos cerámicos.
Se analiza la influencia del método de preparación, usando óxido de lantano o impregnando con nitrato de lantano, variando el número de impregnaciones y la concentración del material activo KOH utilizado. La actividad se determina mediante oxidación a temperatura programada. El catalizador se caracteriza mediante la técnica de Pulsos de CO2 y se analiza la morfología del depósito por microscopía. La estabilidad mecánica del catalizador soportado sobre el monolito se analiza comparando la pérdida de peso del monolito antes y después de ser sometido a una fuerte vibración.
Finalmente, la comparación entre el quemado de hollín proveniente de diesel de petróleo versus hollín proveniente de biodiesel, se realiza mediante la técnica de oxidación a temperatura programada.
EXPERIMENTAL
Preparación de catalizadores en polvo
El catalizador K/La2O3 se preparó mediante impregnación de solución de KOH sobre el soporte La2O3 Alpha, en cantidad necesaria como para obtener un contenido de K de 4.5% w/w. Luego de obtener una pasta, se lo dejó en estufa a 120°C toda la noche y luego se lo calcinó a 400°C.
Preparación de catalizadores soportados sobre el monolito cerámico
Se partió de un monolito comercial, del cual se cortaron porciones de aproximadamente 1 cm3, para realizar las impregnaciones y ensayos de actividad.
El lantano se depositó sobre el monolito cerámico utilizando dos procedimientos. En uno de ellos, se sumerge el monolito en una suspensión de partículas de La2O3 con fuerte agitación. En el otro método, se impregna el monolito con nitrato de lantano. Se varió la cantidad de lantano cambiando el número de impregnaciones, calcinándose luego de cada una de estas a 700ºC. Posteriormente se procede a impregnar el monolito con K (solución KOH de normalidad variable), calcinándose en este caso a 400ºC. En el caso de las preparaciones directas con óxido de lantano, se coimpregna con hidróxido de potasio, siendo calcinado también en este caso a 400ºC. La utilización de una sal soluble de lantano (LaN3O9.6H2O) responde a que se busca formar una capa más fina de óxido de lantano sobre el monolito.
Preparación del hollín
El hollín utilizado en este trabajo se preparó quemando combustible diesel (Repsol-YPF, Argentina) en un recipiente de vidrio. Después de colectarlo de las paredes del recipiente, se secó en estufa a 120°C durante 24 horas.
Ensayos de actividad
La actividad del catalizador, tanto en polvo como depositado sobre el monolito, se determinó por ensayos de oxidación a temperatura programada (TPO). El ensayo se realiza con una mezcla de 5% O2/N2 analizando el CO2 desprendido, producto de la reacción de quemado del hollín con el catalizador. Se usa una técnica modificada, en la cual los gases de salida se transforman cuantitativamente en CH4 y éste se analiza con un FID (detector de ionización de llama). Detalles adicionales pueden verse en (4).
Para medir la actividad del catalizador en polvo se mezclan 20 partes de catalizador con una parte de hollín en un mortero. Se utiliza aproximadamente 10 mg de la mezcla mecánica de catalizador con hollín.
Para medir la actividad de las muestras de catalizador depositado sobre el monolito se sumerge el mismo en una supensión se hollín. El hollín, finamente molido, se suspende en metanol, con el fin de lograr el máximo contacto posible con el catalizador.
La estabilidad térmica de los catalizadores se estudia a través de ciclos de reacción sucesivos (TPO), llegando hasta temperaturas superiores a los 700°C. Luego de cada experiencia de actividad, el monolito se impregna nuevamente en hollín siguiendo exactamente el mismo procedimiento, y usando la misma suspensión de hollín en metanol.
Ensayos de estabililidad del catalizador en polvo frente al SO2
La estabilidad frente al SO2 se analiza sometiendo al catalizador a una corriente de aire con 1000 ppm de SO2 durante 30 horas a 400ºC.
Regeneración del catalizador en polvo
Se utiliza la técnica de reducción a temperatura programada (TPR). En la misma, se somete el catalizador a una rampa de calentamiento de 10°/min mientras fluye por el mismo una corriente de 5% de H2 en Ar. Se utiliza como temperatura final alternativamente 600 y 900°C. La detección se realiza mediante un detector de conductvidad térmica.
Ensayos en microbalanza
Se realizaron en un equipo Cahn 2000 con el objetivo de estudiar la interacción del catalizador con NO + O2. La muestra fue estabilizada a 70°C, punto en el cual se determinó el peso de la muestra (w). Luego, se alimentó una mezcla NO (4%) + O2 (18%) (balance He), y la muestra fue estabilizada a 70°C en este flujo. Cuando se alcanzó un peso constante, la muestra se calentó hasta 490°C a 5°C/min, luego se mantiene a esta temperatura por 10 minutos, y se enfría a 70°C. A esta temperatura la mezcla se cambia a He y se repite el tratamiento térmico que se realizó con NO. Durante toda la experiencia se monitorea el peso.
Ensayos de FTIR (espectroscopía infrarrojo con transformada de Fourier)
Los espectros de infrarrojo se obtuvieron con un espectrómetro Shimadzu 8101M. Las muestras se prepararon en forma de pastillas (aproximadamente 1% muestra diluida en KBr). Todos los espectros involucraron la acumulación de 80 barridos a una resolución de 4 cm-1.
Ensayos de estabililidad del catalizador depositado sobre el monolito frente al SO2
La estabilidad frente al SO2 se analiza sometiendo al monolito con catalizador a una corriente de aire con 1000 ppm de SO2 durante 5,5 horas a 400ºC.
Caracterización del catalizador depositado sobre el monolito cerámico. Ensayos de Pulsos de CO2, Difracción de Rayos X (DRX), Microscopía Óptica y Ensayos de vibración La interacción del CO2 con el catalizador de óxido de lantano promovido con potasio, es bien notable a temperaturas relativamente altas, entre 400 y 500°C. Por este motivo, los catalizadores preparados sobre el monolito se caracterizaron utilizando ensayos de Pulsos de CO2. La experiencia consiste en enviar pulsos de CO2 cada 10 segundos a temperaturas cercanas a las que ocurre la reacción de oxidación del hollín, por ejemplo
500°C, 400°C, 300°C, y realizar calentamientos in situ de la muestra a temperaturas altas, por ejemplo 700°C, seguidamente de pulsos de CO2. El tipo de señal obtenida da información acerca de la fuerza de interacción del CO2 con el catalizador y de la dinámica de adsorción – desorción. A mayor interacción, menor amplitud de la oscilación (5). Se ha propuesto que la reacción de oxidación de hollín procede a través de intermediarios tipo carbonato, para lo cual el catalizador tiene que tener la capacidad de adsorber-desorber el CO2 en las condiciones de reacción (6).
Mediante la observación en el microscopio se analiza la morfología del material final, a fin de analizar si todo el monolito está cubierto por el lantano, y analizar la regularidad del espesor de la película. Puede caracterizarse la influencia del método de preparación en la fracción de superficie cubierta y espesor de la película. Se realizaron experiencias de difracción de rayos X para analizar la composición de la superficie el monolito. Los difractogramas de rayos X se obtuvieron mediante un instrumento Shimadzu XD-D1 con monocromador usando radiación Cu Kα a una velocidad de barrido de 1°/min, desde 2θ = 20 a 100°. También se analizó la estabilidad mecánica de la película de catalizador mediante ensayos en los que se somete el monolito a vibraciones y se mide la pérdida de peso ocasionada por dicha vibración mecánica.
RESULTADOS Y DISCUSIÓN
Catalizador en polvo
El catalizador K(4.5)/La2O3 es activo para la combustión de hollín de diesel. Como se mencionó en otros trabajos la composición de este catalizador es muy compleja ya que depende de su exposición a las condiciones atmosféricas. Las principales fases presentes en el catalizador calcinado a 400°C son La(OH)3 y La2O2CO3. En la Figura 1 se puede observar que dicho catalizador presenta dos máximos en el perfil de TPO, lo que podría significar dos tipos de sitios activos. El tercer pico del perfil de TPO no corresponde a quemado de hollín sino a la descomposición de la especie La2O2CO3 a La2O3, resultado que puede desprenderse de la comparación con experiencias de DSC y TGA realizadas en condiciones similares (7). Para analizar la estabilidad del catalizador frente al SO2 se somete al mismo a una corriente de 1000 ppm de SO2 en aire y se mide actividad mediante la técnica de TPO. De la Figura 1 puede observarse el desplazamiento de los picos de TPO hacia mayores temperaturas al aumentar las horas del tratamiento en SO2.
Es decir que se observa la desactivación progresiva del catalizador, probablemente, y como ocurre en la mayoría de los catalizadores, debido a la formación de especies sulfatos. Con el propósito de regenerar el catalizador, se utiliza la técnica de TPR, es decir, se somete al mismo a una corriente de 5% v/v de H2 en Ar y se le aplica una rampa de calentamiento de 10°/min hasta llegar alternativamente a 600°C y a 900°C. La Figura 1 muestra el resultado de TPO realizado luego del procesos de regeneración a 600°C sobre el catalizador más desactivado (60 hs en SO2). Se puede observar que se recupera actividad aunque la actividad no es tan buena como la inicial, es decir, la correspondiente al catalizador antes de ser envenenado con SO2. El tratamiento a 900°C (no mostrado) no conduce a una más eficiente regeneración, más aún, el segundo pico de TPO está desplazado hacia mayores temperaturas respecto del correspondiente a la regeneración a 600°C. Es decir que llegar a 900°C en la regeneración utilizada no tiene sentido.
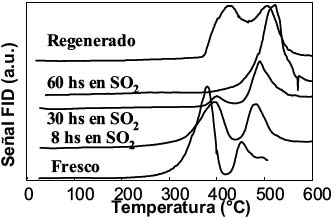 Figura 1: Perfiles de TPO del catalizador sometido a diferentes tratamientos |
Los perfiles de TPR de los catalizadores tratados en SO2 (no mostrados) son similares al correspondiente al La2(SO4)3 (8), mientras que el perfil de TPR realizado en las mismas condiciones para el K2SO4 muestra el inicio de un pico de reducción a una temperatura más alta a las correspondientes a los picos de reducción observados para los catalizadores tratados en SO2. Otro indicio de la reducción de alguna especie sulfato es el olor a H2S que se desprende de la celda luego de la reducción. Es decir que, aparentemente, durante el proceso de regeneración se estaría reduciendo La2(SO4)3 y no sería tan fácil reducir al K2SO4.
Mediante la técnica de FTIR es posible distinguir las especies sulfato. En la Figura 2 se muestran los espectros correspondientes al catalizador fresco, al catalizador envenenado y al catalizador regenerado. La especie K2SO4 presenta tres señales bien claras: 620cm-1, 980 cm-1 y 1120 cm-1. Estas señales aparecen en el catalizador tratado en SO2. Por otra parte se conoce de otros trabajos (9) las señales correspondientes al stretching S-O: 1066 cm-1, 1110 cm-1 y 1155 cm-1 y las señales correspondientes al stretching S=O: 1380 cm-1 y 1480 cm-1. Todas estas señales aparecen en el catalizador tratado en SO2. También aparecen en el catalizador envenenado señales a aproximadamente 605 y 655 cm-1.
Estas señales aparecen también en el La2(SO4)3 (no mostrado). Con todo esto se puede decir que aparentemente el tratamiento en SO2 estaría formando sulfatos de lantano y de potasio. Luego de la regeneración, estas señales persisten aunque con intensidades diferentes. Probablemente, durante el proceso de regeneración se están reduciendo en parte estas especies sulfato.
Si bien el catalizador en estudio es activo para la combustión de hollín, sería deseable que también pueda actuar como trampa de NOx, siendo tanto el hollín como los NOx los contaminantes principales emanados de los motores diesel. Con el propósito de analizar la capacidad de interacción del catalizador con NOx se somete al mismo a una corriente de NO + O2 en una termobalanza y se mide la evolución del peso durante la experiencia.
Luego de someter el catalizador a este tratamiento, cuyo análisis escapa del presente trabajo, se lo analizó mediante FTIR. Figura 3 muestra los espectros de IR de los catalizadores envenenado y regenerado antes y después de la experiencia de adsorción en termobalanza. Luego de ser sometidos a termobalanza los catalizadores muestran las señales de 825 y 1385 cm-1características de las especies nitrato. Y lo que es más interesante aún, es que las señales correspondientes a las especies sulfato disminuyen en intensidad. Probablemente, las especies sulfato estén siendo desplazadas por especies nitrato durante el proceso de adsorción de NO2 en termobalanza. Este dato es muy interesante ya que, en condiciones reales, es decir, con NOx presentes en el ambiente del escape, éstos podrían competir con el SO2 por los sitios activos del catalizador y evitar o reducir el envenenamiento del catalizador con SO2.
 Figura2: Espectros de FTIR de los catalizadores fresco, sulfatado, regenerado y del K2SO4 |
 Figura3: Espectros de FTIR del catalizador sulfatado antes y después de adsorción de NO2 y del catalizador regenerado antes y después de adsorción de NO2 |
Catalizador depositado sobre el monolito cerámico
La Figura 4 muestra los perfiles de TPO de corridas sucesivas correspondientes a un monolito que contiene una impregnación de La2O3 e KOH 0,6 N. Las curvas se muestran tal como se obtuvieron, sin realizar ningún tipo de normalización. Se observa que en los sucesivos ciclos de reacción se produce un desplazamiento del perfil a mayores valores de temperatura, lo que significa que el catalizador va perdiendo actividad. La temperatura final en cada uno de los análisis de TPO estuvo entre 650 y 720ºC. Esto significa que estos tratamientos térmicos producen una pérdida gradual de actividad para el quemado del hollín. El 7º ciclo se realizó después de tratar al monolito con SO2, notándose que no hay una influencia importante en la actividad, obteniéndose prácticamente el mismo perfil que en el 6º ciclo. El SO2 forma sulfatos con los elementos activos del catalizador, que en este caso son, como se demostró en trabajos anteriores, tanto el lantano como el potasio, ambos interviniendo a través de mecanismos con intermediarios tipo carbonato.
Los perfiles de TPO obtenidos con los catalizadores en polvo, y habiéndolos mezclado con el hollín en un mortero, están desplazados a una temperatura considerablemente menor (1). Esto se debe, probablemente, a que el contacto entre las partículas de hollín y el catalizador es mucho mas efectivo en el caso de los catalizadores en polvo, que han sido mezclados trabajándolos mecánicamente con el hollín.
La Figura 1 B muestra los perfiles de TPO obtenidos con el monolito impregnado con nitrato de lantano o con el depósito directo del óxido de lantano, en ambos casos usando solución de KOH 0.6 N. Se observa que el catalizador preparado con el óxido presenta una mejor actividad.
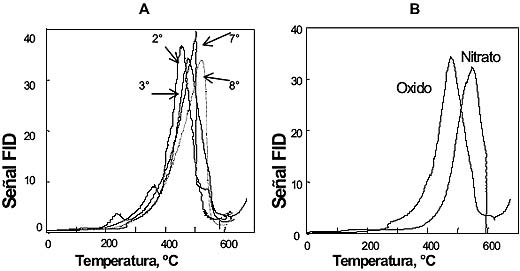 Figura 4: (A) TPO de sucesivos ciclos de reacción efectuados sobre un monolito preparado con La2O3 e KOH, (B) TPO realizados sobre catalizadores preparados con La2O3y con La(NO3)3. |
La Figura 5 muestran un perfil de TPO obtenido con K(10%)/La2O3 en polvo. Se puede apreciar que a bajas temperaturas, el catalizador másico mezclado físicamente con el hollín en un mortero, presenta mayor velocidad de quemado, lo que muestra la importancia de mejorar el contacto efectivo entre el catalizador y el hollín. El catalizador usado en esta experiencia contiene 10% K, habiéndose mostrado en trabajos previos que este porcentaje es excesivamente alto, disminuyendo el efecto promotor del potasio,motivo por el cual se observan picos de alta temperatura. El catalizador con 4 a 7% de K muestra el pico principal bien resuelto con máximo a 350-370°C, sin picos de muy alta temperatura (1). El procedimiento utilizado para contactar el hollín con el catalizador en el caso de los monolitos, corresponde a la peor situación, del tipo contacto ´flojo´. En primer lugar grandes agregados de hollín pueden formarse y depositarse sobre la pared del monolito. Por otro lado el nivel de contacto entre estas partículas y el catalizador es muy pobre. Si bien los perfiles de TPO mostrados en la Figura 4 indican una menor actividad que en el caso de los catalizadores en polvo, no se puede aún determinar el motivo de dicha diferencia, es decir, si la composición lograda es de inferior actividad, o si simplemente el problema del contacto es la causa.
 Figura 5: TPO de K(10%)/ La2O3 + hollín, catalizador en polvo. |
Los Pulsos de CO2 mostrados en la Figura 6 corresponden a un monolito al que se le hicieron dos impregnaciones con nitrato de lantano, calcinando luego de cada una a 700ºC. Se observa que la interacción del catalizador con el CO2 es buena, aumentando con la temperatura. A 500ºC, el catalizador adsorbe todo el CO2, produciendo una señal plana. A temperatura ambiente, la interacción es muy baja, obteniéndose una oscilación con una amplitud muy similar al blanco (sin catalizador), lo que indica que a esta temperatura la adsorción es muy pequeña. El hecho de que la adsorción crezca con la temperatura (menor amplitud de la oscilación a 400ºC que a temperatura ambiente) indica claramente que la interacción entre el CO2 y el catalizador es de tipo químico, formando un compuesto tipo carbonato. Estas experiencias muestran que el lantano ha sido efectivamente depositado sobre el monolito. Se debe tener en cuenta adicionalmente, que el CO2 puede pasar por los canales sin contactarse directamente con la pared de los mismos, por lo que el nivel de interacción indica la presencia de lantano.
 Figura 6: Pulsos de CO2, monolito con 2 impregnaciones de La(NO3)3. |
La Figura 7 muestra una foto de microscopio del depósito de lantano en el monolito cerámico. La Figura 7 A corresponde al caso del depósito realizado impregnando con nitrato de lantano en una etapa, y luego de la calcinación impregnando el potasio. La morfología del depósito es típica de los depósitos realizados con nitrato de lantano. En el caso en que se realizó la impregnación 3 veces consecutivas, se aprecia un mayor espesor de la capa de óxido de lantano luego de las calcinaciones, pero en forma similar a lo mostrado en la Figura 7, sin lograr cubrir absolutamente todo el soporte. En la Figura 7 B se muestra el depósito logrado al aumentar la concentración de KOH de 0.6 a 0.8 N en la solución de impregnación. Notar que la fotografía de la Fig. 7 B se tomo con el doble de aumento que en el caso de la Fig. 7 A. Se observa que el ancho de las grietas del depósito es menor en el caso de una mayor concentración de KOH, lo que probablemente se deba a que el potasio mejora el mojado de la superficie de monolito.
La actividad obtenida con el catalizador correspondiente a la Figura 7 B es notablemente superior al de la Fig. 7 A, lo que se debe a una mayor concentración de potasio en el depósito final. La Figura 8 B muestra los perfiles de TPO de estos dos casos. Se observa la mejor actividad del catalizador preparado con mayor contenido de K. Un aumento posterior de concentración, de 0.8 a 1 N, no produce un aumento adicional de actividad.
Similar observación se tenía con los catalizadores en polvo, en los cuales la actividad de materiales con 4.5 y 7% de K, era muy similar. La Figura 8 A muestra la diferencia en actividad de catalizadores preparados con una y con dos impregnaciones con nitrato de lantano. Se aprecia un leve aumento de la actividad al impregnar dos veces, lo que es consecuencia de una mejor cobertura del monolito con los precursores del lantano.
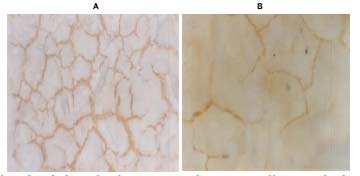 Figura 7: Foto de depósito de lantano sobre monolito cerámico, impregnación con nitrato de lantano, (A) KOH 0.6 N, Aumento: 5 x; (B) KOH 0.8 N, Aumento: 10 x. |
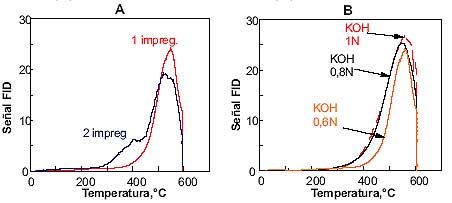 Figura 8: Perfiles de TPO de catalizadores preparados sobre monolitos cerámicos; (A) catalizador con 1 y con 2 impregnaciones con nitrato de La; (B) monolitos impregnados con nitrato de La, y luego con soluciones de KOH de diferentes concentraciones. |
 Figura 9: Difractogramas correspondientes a un monolito sin tratamientos y a un monolito impregnado con catalizador. |
Las curvas que se presentan en la Figura 9 pertenecen a ensayos de difracción de rayos X. La primera curva pertenece a un monolito sin catalizador depositado, en donde no se advierten picos que indicarían difracción en la superficie del mismo. En el segundo caso, la curva fue obtenida a partir de un monolito impregnado con óxido de lantano (calcinado a 900°C) y posteriormente con KOH. El difractograma indica la presencia de fase cristalina de óxido de lantano. Similares espectros fueron obtenidos con catalizadores calcinados a 400°C con diferentes secuencias de preparación.
La gráfica que se muestra en la Figura 10 refleja los distintos ciclos de estabilidad a los que se sometieron los monolitos a través de vibraciones y el posterior registro de la masa. Como se observa, el monolito impregnado con óxido de lantano calcinado a 900°C presenta masa prácticamente invariable, lo que indica elevada estabilidad, esto no ocurre con la misma preparación pero cambiando la temperatura de calcinación a 700°C. En el caso del monolito coimpregnado vemos que su pérdida de masa no es tan importante pero si significativa.
 Figura 10: Ensayos de estabilidad mecánica a los que fueron sometidos diversos monolitos impregnados con catalizador. |
Comparación diesel versus biodiesel
La Figura 11 muestra los perfiles de TPO de dos mezclas mecánicas del catalizador K(4.5)/La2O3 calcinado a 500°C con hollín. En un caso se utilizó hollín de diesel de petróleo y en el otro caso hollín de biodiesel. Este último se generó a partir de un combustible diesel derivado de soja, en las mismas condiciones en que se generó el hollín de diesel de petróleo. De la figura se puede observar que el hollín de biodiesel se quema a menor temperatura que el hollín de diesel.
 Figura 11: Perfiles de TPO de mezcla mecánica catalizador más hollín de diesel y catalizador más hollín de biodiesel. |
CONCLUSIONES
Frente a un ensayo de desactivación acelerado con 1000 ppm SO2 en aire, el catalizador K/La2O3 se desactiva con formación de sulfatos de potasio y de lantano. Luego de someterlo a un proceso de regeneración con H2 a 600°C se recupera actividad, aunque no se alcanza el valor de actividad correspondiente al catalizador sin envenenar.
Por otra parte, luego de someter el catalizador a una corriente de NO y O2, las especies nitrato podrían estar desplazando en parte las especies sulfato del catalizador, lo cual se observa a partir de la disminución de intensidad de las señales de IR correspondientes a las especies sulfatos. Estos resultados son preliminares.
Al depositar el catalizador sobre un monolito cerámico, se observa un comportamiento superior en adherencia cuando se usa nitrato de lantano como precursor de lantano.
Cuando se usa directamente óxido de lantano como precursor de lantano, se observan mayores zonas de monolito no cubiertas con catalizador, es decir, menor resistencia mecánica, pero mayor actividad que cuando se usa nitrato de lantano como precursor. En ambos casos ocurre un corrimiento progresivo de las curvas de TPO hacia mayores temperaturas al realizar sucesivos ciclos de reacción, probablemente debido a pérdidas mecánicas de la capa de catalizador que recubre el monolito. Luego del tratamiento con SO2 la actividad prácticamente no se modificó, pero se debe tener en cuenta que el tratamiento se realizó luego de varios ciclos, estando ya el sistema catalítico con baja actividad.
En cualquiera de los dos casos, la actividad del catalizador depositado sobre el monolito ya no es tan buena como la correspondiente a la del catalizador en polvo y mezclado mecánicamente con el hollín, ya que en este último caso el contacto catalizadorparticulado es más íntimo.
Finalmente, al analizar la actividad de catalizadores frente a la combustión de distintos tipos de hollín, se observó que el combustible biodiesel quema a menor temperatura que el combustible diesel.
Actualmente se está trabajando en mejorar la adherencia catalizador-monolito. También se está estudiando la regeneración del catalizador envenenado con SO2.
REFERENCIAS
(1) M.L. Pisarello, V.G. Milt, M.A. Peralta, C.A. Querini, E.E. Miró, Catalysis Today 75, 465 (2002)
(2) C.A. Querini, L.M. Cornaglia, M.A. Ulla, E.E. Miró; Applied Catalysis B: Enviromental 20 (1999) 165-177.
(3) M.L. Pisarello, C. Saux,M.A. Peralta, C.A. Querini, E.E. Miró; Proc. ENPROMER 2001 11 (2001) 1087-1092.
(4) S. C. Fung, C.A.Querini, Journal of Catálisis 138 (1992) 240-254.
(5) V.G. Milt, M.L. Pisarello, E.E. Miró, C.A.Querini – Applied Catálisis B: Environmental 41 (2003) 397-414
(6) V.G. Milt, C.A. Querini, E.E. MIró, M.A. Ulla, J. Catal. 220( 2003) 424-432
(7) V. Milt, C.A. Querini, E.E.Miró. Thermochimica Acta 404 (2003) 177
(8) Y. Zhang-Steenwinkel, H.L.Casticum, J.Beckers, E.Eiser, A.Bliek. Journal of Catalysis 221 (2004) 523-531
(9) I. Rosso, E.Garrone, F.Geobaldo, B.Onida, G.Saracco, V.Specchia. Applied Catalysis B. Environmental 30 (2001) 61-73
Por: M. Ariela Peralta, M. José Fernández, M. Alicia Ulla, Carlos A. Querini
Instituto de Investigaciones en Catálisis y Petroquímica (INCAPE)
Fuente: Revista Petroquímica